
 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:高中化学 来源: 题型:
Mg、Cu和Al三种金属粉末的混合物,加入过量盐酸充分反应,过滤后向滤液中加入过量NaOH溶液,再过滤,滤液中存在的离子有( )
A.AlO2- B.Al3+ C.Mg2+ D.Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是
A. 12g石墨烯(单层石墨)中含有六元环的个数为0.5NA
B.25℃时pH=13的NaOH溶液中含有OH一的数目为0.1 NA
C.1mol的羟基与1 mol的氢氧根离子所含电子数均为9 NA
D.1.0L1.5mo1·L-1的NaAlO2水溶液中含有的氧原子数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
 短周期元素A、B、C、D在周期表中的位置如图所示,B、D最外层电子数之和为12,二者可形成
短周期元素A、B、C、D在周期表中的位置如图所示,B、D最外层电子数之和为12,二者可形成 两种分子,
两种分子, 具有漂白性。回答下列问题:
具有漂白性。回答下列问题:
(1)A的氢化物的电子式是____________。
(2)请写出能证明C、D非金属必强弱的化学方程式______。
(3)硒(Se)是人体必需的微量元素,与元素B、D同一主族,该族第2~5周期元素单质分别与 反应生成1 mol气态氢化物对应的热量变化如下,其中能表示生成1 mol硒化氢所对应的热量变化是_______(选填字母编号)。
反应生成1 mol气态氢化物对应的热量变化如下,其中能表示生成1 mol硒化氢所对应的热量变化是_______(选填字母编号)。
a.吸收99.7kJ b.吸收29.7kJ c.放出20.6kJ d.放出241.8
(4) 通过下列工艺流程可制化工业原料
通过下列工艺流程可制化工业原料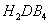 和清洁能源
和清洁能源 。
。

①为检验分离器的分离效果,取分离后的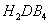 溶液于试管,向其中逐滴加入
溶液于试管,向其中逐滴加入 溶液至充分反应,若观察到________________,证明分离效果较好。
溶液至充分反应,若观察到________________,证明分离效果较好。
②在原电池中,负极发生的反应式为___________________________。
③在电解过程中,电解槽阴极附近溶液pH_______(填“变大”、“变小”或“不变”)
④将该工艺流程用反应的化学方程式表示为:________,该生产工艺的优点有________(答一点即可);缺点有___________(答一点即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
0.1 mol·L-1Ba(OH)2溶液与0.1 mol·L-1的铵明矾[NH4Al(SO4)2]溶液等体积混合,反应后混合液各离子浓度大小比较合理的是( )
A.c(SO42-)>c(NH4+)>c(Al3+)>c(OH-)>c(H+)
B.c(SO42-)>c(NH4+)>c(Al3+)>c(H+)>c(OH-)
C.c(NH4+)>c(SO42-)>c(Al3+)>c(OH-)>c(H+)
D.c(SO42-)>c(Al3+)>c(NH4+)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
三种短周期元素A、B和C,它们的原子序数是依次增大,其中C的原子半径在短周期的主族元素中最大,B和C的最外层电子数之和等于A的最外层电子数的2倍,且A是构成有机物的重要元素,下列说法正确的是( )
A.A元素位于元素周期表中第二周期ⅥA族
B.B离子与C离子具有相同的电子层结构
C.C离子具有很强的还原性,B离子具有很强的氧化性
D.B、C可以形成BC2型化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
下列比较关系与排列顺序错误的是
A.酸性 H4SiO4<H3PO4<H2SO4<HClO4 B.碱性 Ca(OH)2>Mg(OH)2>Al(OH)3
C.稳定性SiH4>NH3>H2O>HF D.半径 O2->F->Mg2+>Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列表格中各项分类都正确的一组是:( )
|
选项 | 纯净物 | 混合物 | 电解质 | 非电解质 |
| A | 生理盐水 | 明矾 | 液态KNO3 | 蔗糖 |
| B | CaO | 海 水 | 铜 | 乙醇 |
| C | 胆矾 | 铝合金[ | AgCl | CO2 |
| D | 氢氧化钠 | 空气 | Na2SO4溶液 | 食醋 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com