
【题目】甲乙两同学对保存已久的Na2SO3试剂进行试验探究。取适量Na2SO3样品于洁净烧杯中,加入适量蒸馏水,充分搅拌全部溶解。
(1)测上述溶液的PH值,其PH值>7,原因是(用离子方程式表示)_____________________________________
(2)取少量上述溶液于试管中,加入硝酸钡溶液生成白色沉淀,再加入盐酸,白色沉淀不溶解,甲认为已变质,乙认为他的结论不科学,理由是________________________________
(3)假设试剂由Na2SO3和Na2SO4组成,设计试验方案,进行成分检验,他们决定继续探究,请写出实验步骤、预期现象和结论。
限选试剂及仪器:稀盐酸、稀硝酸、氯化钡溶液,品红溶液,酸性高锰酸钾溶液,NaOH溶液、澄清石灰水、pH计、烧杯、试管、带塞导气管、滴管
实验步骤 | 预期现象和结论 |
步骤1:取适量试剂于洁净烧杯中,加入足量蒸馏水,充分搅拌,静置。 | |
步骤2:取适量步骤1所得溶液于试管中 加入少量的____________________溶液。 | 若溶液褪色,说明其有_________若溶液不褪色,说明其中没有______ |
步骤3: 再取适量步骤1所得溶液于另一试管中,先加入足量的稀盐酸,再滴 加___________溶液。 | 如果有白色沉淀生成,则说明其中有_____________,已经变质。 如果没有白色沉淀生成,则说明其中 没有_____________ |
(4)经实验检验后,确实已变质,现准确测定其中Na2SO3的含量。实验如下:
①配制250ml 约0.2molL-1 Na2SO3溶液:准确称取w克试样,置于烧杯中,加适量蒸馏水溶解,将溶液转入____________,洗涤,定容,摇匀。
②滴定:准确量取25.00ml Na2SO3所配制溶液于锥形瓶中,将 0.05molL-1酸性高锰酸钾装入50ml__________(填酸式或碱式)滴定管,滴定至终点,记录数据。重复滴定2次。平均消耗KMnO4VmL。
③计算Na2SO3的质量分数=______________(只列出计算式,不要求算出结果)
【答案】 SO32-+H2O![]() HSO3-+OH- 溶液中的NO3-和H+在一起有强氧化性,会把亚硫酸钡氧化成硫酸钡 酸性高锰酸溶液 Na2SO3 Na2SO3 氯化钡 Na2SO4 Na2SO4 250mL容量瓶 酸式 计算Na2SO3的质量分数=5×0.05×10×126V/2000W×100%
HSO3-+OH- 溶液中的NO3-和H+在一起有强氧化性,会把亚硫酸钡氧化成硫酸钡 酸性高锰酸溶液 Na2SO3 Na2SO3 氯化钡 Na2SO4 Na2SO4 250mL容量瓶 酸式 计算Na2SO3的质量分数=5×0.05×10×126V/2000W×100%
【解析】试题分析:(1)Na2SO3是强碱弱酸盐,水解显碱性,所以Na2SO3溶液pH>7的原因是SO32-+H2O![]() HSO3-+OH-。
HSO3-+OH-。
(2)溶液中的NO3-和H+在一起有强氧化性,会把亚硫酸钡氧化成硫酸钡,所以在亚硫酸钠溶液中加入硝酸钡溶液生成白色沉淀,再加入盐酸,白色沉淀不溶解,并不能说明Na2SO3已经变质。
(3)酸性高猛酸钾溶液具有氧化性,能将Na2SO3氧化成Na2SO4,高猛酸钾因发生还原反应而褪色,所以取适量步骤1所得溶液于试管中,加入少量的酸性高锰酸溶液,若酸性高锰酸溶液褪色,说明中有Na2SO3,相反,若酸性高锰酸溶液不褪色,说明中没有Na2SO3。因为BaSO3能溶于盐酸,而BaSO4不溶于盐酸,所以再取适量步骤1所得溶液于另一试管中,先加入足量的稀盐酸,再滴加氯化钡溶液,如果有白色沉淀生成,则说明其中有Na2SO4,已经变质;如果没有白色沉淀生成,则说明没有Na2SO4。
(4)①因为需要配制250mL的溶液,所以选择250mL容量瓶;
②高猛酸钾具有氧化性,能腐蚀橡胶,所以将高猛酸钾酸性溶液盛装在酸式滴定管中。
③根据化学反应5Na2SO3+2KMnO4+H2SO4=5Na2SO4+2MnSO4+H2O+K2SO4, Na2SO3的质量分数="5×0.05×10×126V/2000W×100%" 。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 1mol 有机物 在一定条件下能和7mol NaOH 反应
在一定条件下能和7mol NaOH 反应
B. 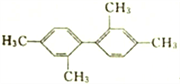 分子中至少有11个碳原子处于同一平面上
分子中至少有11个碳原子处于同一平面上
C. 分子式为C4H7ClO2,可与NaHCO3 产生CO2的有机物的结构可能有3 种
D. 甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科研人员设计一种电化学反应器以Na2SO4溶液为电解质,负载纳米MnO2的导电微孔钛膜和不锈钢为电极材料。这种电催化膜反应器可用于正丙醇合成丙酸,装置示意图:

以下叙述错误的是
A. 微孔钛膜作阴极
B. 使用Na2SO4溶液是为了在电解开始时增强溶液导电性
C. 丙醇转化为丙酸的电极反应式为:CH3CH3CH2OH+H2O-4e-=CH3CH2COOH+4H+
D. 反应器工作时料槽中正丙醇分子向电催化膜移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.其他条件不变时增大压强,能使全气体反应体系中活化分子百分数增加
B.中和反应都是放热反应
C.在FeCl3溶液和KSCN溶液反应的平衡体系中,加入KCl固体,平衡逆向移动
D.熵增大的反应不一定自发,但自发反应熵一定增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃时,Ksp(AgCl)=1.8×10-10,Ksp(AgBr)=5.0×10-13。该温度下,下列说法错误的是
A. AgCl的悬浊液中通入少量HCl,c(Ag+)减小
B. AgCl和AgBr共存的悬浊液中,c(Cl-)/c(Br-)=360
C. AgBr悬浊液中加入足量NaCl可能有AgCl沉淀生成
D. 等浓度的NaCl和NaBr混合溶液中滴加AgNO3溶液,先析出AgCl沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知浓度均为0.1 mol/L的8种溶液:①CH3COONa、②KCl、③NH4Cl 、④NaOH 、⑤Ba(OH)2、⑥HNO3、⑦H2SO4、⑧CH3COOH,其溶液的pH由小到大的顺序是__________________________(填写序号)。
(2)25℃时,若体积为Va、pH=a的某一元强酸溶液与体积为Vb、pH=b的某一元强碱溶液混合,恰好中和。请回答:
若a+b=12,则Va: Vb=________。
若Va<Vb和a=0.5b,则a的取值范围是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.1 molH2的质量是1 g
B.1 mol HCl的质量是36.5 gmol﹣1
C.Cl2的摩尔质量等于它的相对分子质量
D.硫酸根离子的摩尔质量是96 gmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳是一种常见的元素,它以多种形式广泛存在于自然界之中。
(1)星际空间存在多种有机分子和无机分子,多数都含有碳元素,C2是一种星际分子,C2和C60互为_______________。
(2)CO2是碳元素重要的氧化物,回答下列有关问题:
①利用CO2与Na2O2反应,可向呼吸面具中提供氧气,其反应方程式为_________________。
②工业上可由CO2和NH3在一定条件下合成尿素,反应方程式为2NH3+CO2![]() CO(NH2)2+H2O当
CO(NH2)2+H2O当![]() 时,CO2的转化率随时间的变化关系如图所示.
时,CO2的转化率随时间的变化关系如图所示.
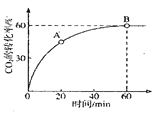
A点的逆反应速率![]() __________B点的正反应速率
__________B点的正反应速率![]() (填“大于“小于”或“等于”),NH3的平衡转化率为____________。
(填“大于“小于”或“等于”),NH3的平衡转化率为____________。
③随着对环境问题认识的深入,CO2的转化捕获问题已成为科研热点之一,以附着纳米银的惰性电极作阴极,可电解CO2转化为CO,装置示意图如下:
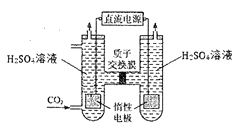
写出通CO2侧电极反应式_________________。
④CO2可用于生产碳酸饮料。苯甲酸钠(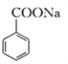 可写为C6H5COONa)也是某些饮料的添加剂,具有抑菌防腐的作用。研究表明苯甲酸(C6H5COOH)的抑菌能力显著高于苯甲酸钠。在生产的某饮料的过程中,除了添加苯甲酸钠外,还需加压充入CO2气体。若忽略碳酸的二级电离,试写出碳酸与苯甲酸钠反应的离子方程式__________________,经计算该反应的化学平衡常数为______________,加压充入CO2后,该饮料的抑菌能力明显增强,结合上述离子方程式分析其原因_______________(已知:H2CO3的Ka1=4.17×10-7;C6H5COOH的Ka=6.25×10-5。)。
可写为C6H5COONa)也是某些饮料的添加剂,具有抑菌防腐的作用。研究表明苯甲酸(C6H5COOH)的抑菌能力显著高于苯甲酸钠。在生产的某饮料的过程中,除了添加苯甲酸钠外,还需加压充入CO2气体。若忽略碳酸的二级电离,试写出碳酸与苯甲酸钠反应的离子方程式__________________,经计算该反应的化学平衡常数为______________,加压充入CO2后,该饮料的抑菌能力明显增强,结合上述离子方程式分析其原因_______________(已知:H2CO3的Ka1=4.17×10-7;C6H5COOH的Ka=6.25×10-5。)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金刚石和石墨均为碳的同素异形体,氧气不足时它们燃烧生成一氧化碳,充分燃烧时生成二氧化碳,反应中放出的热量如图所示。

(1)写出石墨转化为金刚石的热化学方程式____________________________________。
(2)写出石墨和二氧化碳反应生成一氧化碳的热化学方程式_____________________。
(3)科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。反应过程的示意图如下:
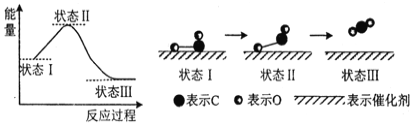
①判断CO和O生成CO2是放热反应的依据是__________________。
②写出CO2的电子式___________________,CO2含有的化学键类型是(若含共价键,请标明极性或非极性)______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com