
 人体中含量位于前6名的元素依次是:氢、氧、X、氮、钙、磷.根据要求用以上元素完成下列填空:
人体中含量位于前6名的元素依次是:氢、氧、X、氮、钙、磷.根据要求用以上元素完成下列填空: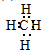 ;该分子的空间构型为正四面体结构.
;该分子的空间构型为正四面体结构.分析 (1)人体中含量位于前6名的元素依次是:氧、碳、氢、氮、钙、磷;
s能级的电子云为球形,能量最高的亚层电子云呈球形,说明该元素最高能级为ns;
(2)形成化合物种类最多的元素为C元素,最简氢化物为CH4,分子中C原子与H原子之间形成1对共用电子对,为正四面体结构,为非极性分子;
(3)a.氧元素没有含氧酸;
b.单质与H2反应的难易程度,说明单质的氧化性强弱,单质的结构不同,不能说明元素的非金属性;
c.NO2、CO2和C3N4中元素的化合价,说明共用电子对偏移方向,化合物中表现负价的元素,对键合电子的吸引力更强,非金属性更强;
d.非金属性越强,气态氢化物越稳定;
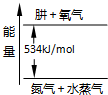
(4)由肼燃烧时的能量变化图可知,1mol肼燃烧生成氮气与水蒸气,放出的热量为534kJ,据此热化学方程式书写原则书写.
解答 解:(1)人体中含量位于前6名的元素依次是:氧、碳、氢、氮、钙、磷,故X为H元素,s能级的电子云为球形,能量最高的亚层电子云呈球形,说明该元素最高能级为ns,符合条件的有H、Ca,故答案为:H;H、Ca;
(2)形成化合物种类最多的元素为C元素,最简氢化物为CH4,分子中C原子与H原子之间形成1对共用电子对,电子式为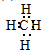 ,为正四面体结构,分子中正负电荷的重心重合,为非极性分子,故答案为:
,为正四面体结构,分子中正负电荷的重心重合,为非极性分子,故答案为: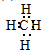 ;正四面体结构;
;正四面体结构;
(3)a.氧元素没有含氧酸,不能利用最高价比较氧元素与C、N元素的非金属性,故a错误;
b.单质与H2反应的难易程度,说明单质的氧化性强弱,单质的结构不同,不能说明元素的非金属性,故b错误;
c.化合价说明共用电子对偏移方向,化合物中表现负价的元素,对键合电子的吸引力更强,非金属性更强,故NO2中氧元素为-2价,氧元素吸引电子能力更强,故非金属性O>N,CO2中,中氧元素为-2价,氧元素吸引电子能力更强,故非金属性O>C,C3N4中N元素为-3价,N元素吸引电子能力更强,故非金属性N>O,可以比较,故c正确;
d.非金属性越强,气态氢化物越稳定,故气态氧化物的稳定性可以比较非金属性强弱,故d正确;
故答案为:cd;
(4)由肼燃烧时的能量变化图可知,1mol肼燃烧生成氮气与水蒸气,放出的热量为534kJ,热化学方程式为N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-534kJ/mol,
故答案为:N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-534kJ/mol.
点评 本题考查原子结构及元素周期律,为高频考点,把握元素的含量、元素非金属性、热化学方程式、元素周期律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.


 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源: 题型:选择题
| A. | 12 g石墨和C60的混合物中质子总数为6NA | |
| B. | 常温下,4g 14CH4含有NA个C-H共价键 | |
| C. | 25℃时,pH=12的1.0 L NaClO溶液中水电离出的OH-的数目为0.01NA | |
| D. | 0.1 mol•L-1 Na2CO3溶液中含有0.1NA个CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从1L 1 mol•L-1的氯化钠溶液中取出10ml,其浓度仍是1 mol•L-1 | |
| B. | 物质的量是指物质所含微粒的数目 | |
| C. | 0.5 L 2 mol•L-1的氯化钡溶液中,钡离子和氯离子总数为3×6.02×1023 | |
| D. | 冰水混合物既是纯净物又是化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等物质的量的H2O与D2O含有的中子数 | |
| B. | 等质量的乙烯和丙烯中含有的共用电子对数 | |
| C. | 同温、同压、同体积的CO和NO含有的质子数 | |
| D. | 等物质的量的镁和铝分别与足量氯气完全反应时转移的电子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸工业中涉及的3步反应都为氧化还原反应 | |
| B. | 由反应:H2S+Cl2═S↓+2HCl可知,还原性:Cl2>S | |
| C. | 如用NaOH溶液来吸收尾气中的SO2,只能生成一种盐 | |
| D. | 常温下,铝质容器或铁质容器可储运浓硫酸和浓硝酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
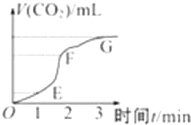 用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,请回答:
用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度(℃) | SO2起始浓度(mol•L-1) | O2起始浓度(mol•L-1) | 平衡时SO3 体积分数(%) |
| T1 | 2 | 1 | ω1 |
| T1 | 4 | 2 | ω2 |
| T2 | 4 | 2 | ω1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2H2(g)+O2(g)=2H2O(l)△H1 2H2(g)+O2(g)=2H2O(g)△H2 | |
| B. | S(g)+O2(g)=SO2(g)△H1 S(s)+O2(g)=SO2(g)△H2 | |
| C. | C(s)+O2(g)=CO(g)△H1 C(s)+O2(g)=CO2(g)△H2 | |
| D. | H2(g)+Cl2(g)=2HCl(g)△H1 $\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)=HCl(g)△H2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com