
”¾ĢāÄæ”æÓÉĻĀĮŠŹµŃé¼°ĻÖĻó²»ÄÜĶĘ³öĻąÓ¦½įĀŪµÄŹĒ
ŹµŃé | ĻÖĻó | ½įĀŪ | |
A. | Ļņ | »ĘÉ«Öš½„ĻūŹ§£¬¼Ó | »¹ŌŠŌ£ŗ |
B. | ½«½šŹōÄĘŌŚČ¼ÉÕ³×ÖŠµćČ¼£¬ŃøĖŁÉģČė¼ÆĀś | ¼ÆĘųĘæÖŠ²śÉś“óĮæ°×ŃĢ£¬ĘæÄŚÓŠŗŚÉ«æÅĮ£²śÉś |
|
C. | ½«×ćĮæµÄ | ĖįŠŌ |
|
D. | ½« | ĻČÓŠ°×É«³ĮµķÉś³É£¬ŗó±äĪŖĄ¶É«³Įµķ |
|
A.AB.BC.CD.D
”¾“š°ø”æC
”¾½āĪö”æ
A£®FeCl3µÄČÜŅŗÖŠ¼Ó×ćĮæĢś·Ū£¬»ĘÉ«Öš½„ĻūŹ§£¬¼ÓKSCNČÜŅŗŃÕÉ«²»±ä£¬ĖµĆ÷·“Ӧɜ³ÉĮĖĀČ»ÆŃĒĢś£¬Äܹ»ĖµĆ÷»¹ŌŠŌ£ŗFe£¾Fe2+£¬¹ŹAÕżČ·£»
B£®ÄĘÓė¶žŃõ»ÆĢ¼·“Ó¦£¬¼ÆĘųĘæÖŠ²śÉś“óĮæ°×ŃĢ£¬ĘæÄŚÓŠŗŚÉ«æÅĮ£²śÉś£¬ĖµĆ÷Éś³ÉĮĖĢ¼ĖįÄĘ”¢C£¬ĖµĆ÷CO2¾ßÓŠŃõ»ÆŠŌ£¬¹ŹBÕżČ·£»
C£®ŃĒĢśĄė×Ó¼°¹żĮæµÄ¶žŃõ»ÆĮņ¾łŹ¹øßĆĢĖį¼ŲČÜŅŗĶŹÉ«£¬ÓÉĻÖĻó²»ÄÜĖµĆ÷SO2ÓėFeCl3·¢ÉśĮĖŃõ»Æ»¹Ō·“Ó¦£¬¹ŹC“ķĪó£»
D£®ĻČÓŠ°×É«³ĮµķÉś³É£¬ŗó±äĪŖĄ¶É«³Įµķ£¬ĖµĆ÷·¢ÉśĮĖ³ĮµķµÄ×Ŗ»Æ£¬ÓÉĻÖĻóæÉÖŖKsp[Cu(OH)2]£¼Ksp[Mg(OH)2]£¬¹ŹDÕżČ·£»
¹ŹŃ”C”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČżĮņ“śĢ¼ĖįÄĘ(Na2CS3)³£ÓĆ×÷ɱ¾ś¼Į”¢³Įµķ¼Į”£Ä³Š”×éÉč¼ĘŹµŃéĢ½¾æČżĮņ“śĢ¼ĖįÄʵĊŌÖŹ²¢²ā¶ØĘäČÜŅŗµÄÅØ¶Č”£
ŹµŃé1£ŗĢ½¾æNa2CS3µÄŠŌÖŹ
²½Öč | ²Ł×÷¼°ĻÖĻó |
¢Ł | ȔɣĮæNa2CS3¹ĢĢåČÜÓŚÕōĮóĖ®ÅäÖĘ³ÉČÜŅŗ²¢·Ö³ÉĮ½µČ·Ż |
¢Ś | ĻņĘäÖŠŅ»·ŻČÜŅŗÖŠµĪ¼Ó¼øµĪ·ÓĢŖŹŌŅŗ£¬ČÜŅŗ±äŗģÉ« |
¢Ū | ĻņĮķŅ»·ŻČÜŅŗÖŠµĪ¼ÓĖįŠŌKMnO4ČÜŅŗ£¬×ĻÉ«ĶŹČ„ |
£Ø1£©H2CS3ŹĒ________Ėį£ØĢī”°Ēæ”±»ņ”°Čõ”±£©”£
£Ø2£©ŅŃÖŖ²½Öč¢ŪµÄŃõ»Æ²śĪļŹĒSO42£,Š“³öøĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½______
£Ø3£©Ä³Ķ¬Ń§Č”²½Öč¢ŪĖłµĆČÜŅŗÓŚŹŌ¹ÜÖŠ£¬µĪ¼Ó×ćĮæŃĪĖį”¢BaCl2ČÜŅŗ²śÉś°×É«³Įµķ£¬ĖūČĻĪŖĶعż²ā¶Ø²śÉśµÄ°×É«³ĮµķµÄÖŹĮ漓æÉĒó³öŹµŃéĖłÓĆNa2CS3µÄĮ棬ÄćŹĒ·ńĶ¬ŅāĖūµÄ¹Ūµć²¢ĖµĆ÷ĄķÓÉ______”£
ŹµŃé2£ŗ²ā¶ØNa2CS3ČÜŅŗµÄÅضČ

°“ČēĶ¼ĖłŹ¾Į¬½ÓŗĆ×°ÖĆ£¬Č”100mLNa2CS3ČÜŅŗÖĆÓŚČż¾±ÉÕĘæÖŠ£¬“ņæŖŅĒĘ÷dµÄ»īČū£¬µĪČė×ćĮæ2.0mol/LĻ”H2SO4£¬¹Ų±Õ»īČū”£
ŅŃÖŖ£ŗNa2CS3 + H2SO4=Na2SO4 + CS2 + H2S”ü”£CS2ŗĶH2S¾łÓŠ¶¾”£CS2²»ČÜÓŚĖ®£¬·Šµć46”ę£¬ÓėCO2ijŠ©ŠŌÖŹĻąĖĘ£¬ÓėNaOH×÷ÓĆÉś³ÉNa2COS2ŗĶH2O”£
£Ø4£©Ź¢·ÅĪŽĖ®CaCl2µÄŅĒĘ÷µÄĆū³ĘŹĒ______£¬BÖŠ·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ______”£
£Ø5£©·“Ó¦½įŹųŗó“ņæŖ»īČūk£¬ŌŁ»ŗĀżĶØČėČČN2Ņ»¶ĪŹ±¼ä£¬ĘäÄæµÄŹĒ______”£
£Ø6£©ĪŖĮĖ¼ĘĖćNa2CS3ČÜŅŗµÄÅØ¶Č£¬¶ŌBÖŠ»ģŗĻĪļ½ųŠŠ¹żĀĖ”¢Ļ“µÓ”¢øÉŌļ”¢³ĘÖŲ£¬µĆ19.2g¹ĢĢ壬ŌņAÖŠNa2CS3µÄĪļÖŹµÄĮæÅضČĪŖ______”£
£Ø7£©·ÖĪöÉĻŹöŹµŃé·½°ø£¬»¹æÉŅŌĶعż²ā¶ØCÖŠČÜŅŗÖŹĮæµÄŌö¼ÓÖµĄ“¼ĘĖćNa2CS3ČÜŅŗµÄÅØ¶Č£¬Čō·“Ó¦½įŹųŗó½«ĶØČČN2øÄĪŖĶØČČæÕĘų£¬¼ĘĖćÖµ______£ØĢī”°Ę«øß”±”¢”°Ę«µĶ”±»ņ”°ĪŽÓ°Ļģ”±£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆĻĀĮŠŹµŃé×°ÖĆĶź³É¶ŌÓ¦µÄŹµŃé(²æ·ÖŅĒĘ÷ŅŃŹ”ĀŌ)£¬ÄÜ“ļµ½ŹµŃéÄæµÄµÄŹĒ£Ø””””£©
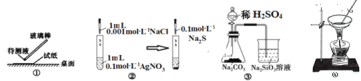
A.¢ŁÓĆpHŹŌÖ½²āijČÜŅŗµÄĖį¼īŠŌ
B.ŹµŃéŹŅÓĆĶ¼¢ŚĖłŹ¾×°ÖĆČōĻČ³öĻÖ°×É«³ĮµķŗóÓÖ±äŗŚ£¬ŌņÄÜ±Č½ĻKsp(AgCl)©Ksp(Ag2S)
C.ŹµŃéŹŅÓĆĶ¼¢ŪĖłŹ¾×°ÖĆÖ¤Ć÷ĖįŠŌ£ŗH2SO4>H2CO3>H2SiO3
D.Ķ¼¢ÜæÉÓÉAlCl3±„ŗĶČÜŅŗÖʱøAlCl3¾§Ģå
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ2019ÄźÅµ±“¶ū»Æѧ½±°äøųĮĖČżĪ»ĪŖļ®Ąė×Óµē³Ų·¢Õ¹×÷³öÖŲŅŖ¹±Ļ×µÄæĘѧ¼Ņ”£Į×ĖįĢśļ®ļ®Ąė×Óµē³Ų³äµēŹ±Ńō¼«·“Ó¦Ź½ĪŖ,![]() £¬·Åµē¹¤×÷Ź¾ŅāĶ¼ČēĶ¼”£ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ
£¬·Åµē¹¤×÷Ź¾ŅāĶ¼ČēĶ¼”£ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ
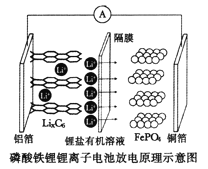
A.·ÅµēŹ±£¬Li+ĶعżøōĤŅĘĻņÕż¼«
B.·ÅµēŹ±£¬µē×ÓÓÉĀĮ²ŃŲµ¼ĻßĮ÷ĻņĶ²
C.·ÅµēŹ±Õż¼«·“Ó¦ĪŖ£ŗ![]()
D.Į×ĖįĢśļ®ļ®Ąė×Óµē³Ų³ä·Åµē¹ż³ĢĶعżLi+ĒØŅĘŹµĻÖ£¬C”¢Fe”¢PŌŖĖŲ»ÆŗĻ¼Ū¾ł²»·¢Éś±ä»Æ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄæĒ°£¬“¦ĄķŃĢĘųÖŠ SO2 ³£²ÉÓĆĮ½ÖÖ·½·Ø£ŗ¼īŅŗĪüŹÕ·ØŗĶĖ®ĆŗĘų»¹Ō·Ø”£
¢ń.¼īŅŗĪüŹÕ·Ø
25”ꏱ£¬Kb(NH3”¤H2O)£½1.8”Į10£5£»H2SO3£ŗKa1£½1.5”Į10£2£¬Ka2£½1.0”Į10£7£»Ksp(CaSO4)£½7.1”Į10£5”£
µŚ1²½£ŗÓĆ¹żĮæµÄÅØ°±Ė®ĪüŹÕ SO2£¬²¢ŌŚæÕĘųÖŠŃõ»Æ£»
µŚ2²½£ŗ¼ÓČėŹÆ»ŅĖ®£¬·¢Éś·“Ó¦ Ca2£«£«2OH££«2NH4£«£«SO42£CaSO4”ż£«2NH3”¤H2O K”£
(1)25”ꏱ£¬0.1 mol”¤L£1(NH4)2SO3 ČÜŅŗµÄ pH_____(Ģī”°>”±”°<”±»ņ”°£½”±)7”£
(2)¼ĘĖ浌2²½ÖŠ·“Ó¦µÄ K£½_____”£
¢ņ.Ė®ĆŗĘų»¹Ō·Ø
ŅŃÖŖ£ŗ¢Ł2CO(g)£«SO2(g)=S(l)£«2CO2(g) ¦¤H1£½£37.0 kJ”¤mol£1
¢Ś2H2(g)£«SO2(g)=S(l)£«2H2O(g) ¦¤H2£½£«45.4 kJ”¤mol£1
¢ŪCO µÄČ¼ÉÕČȦ¤H3£½£283 kJ”¤mol£1
(3)±ķŹ¾ŅŗĢ¬Įņ(S)µÄČ¼ÉÕČȵÄČČ»Æѧ·½³ĢŹ½ĪŖ_________”£
(4)·“Ó¦¢ŚÖŠ£¬Õż·“Ó¦»ī»ÆÄÜ E1_____(Ģī”°>”±”°<”±»ņ”°£½”±)¦¤H2”£
(5)ŌŚŅ»¶ØŃ¹ĒæĻĀ£¬·¢Éś·“Ó¦¢Ł”£Ę½ŗāŹ±SO2µÄ×Ŗ»ÆĀŹ¦Į(SO2)ÓėĶ¶ĮĻ±ČµÄ±ČÖµ[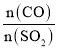 £½y]”¢ĪĀ¶Č T µÄ¹ŲĻµČēĶ¼ĖłŹ¾”£
£½y]”¢ĪĀ¶Č T µÄ¹ŲĻµČēĶ¼ĖłŹ¾”£
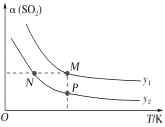
±Č½ĻĘ½ŗāŹ±COµÄ×Ŗ»ÆĀŹ¦Į(CO)£ŗN_____M”£Äę·“Ó¦ĖŁĀŹ£ŗN_____P(Ģī”°>”±”°<”±»ņ”°£½”±)”£
(6)ijĪĀ¶ČĻĀ£¬Ļņ10LŗćČŻĆܱÕČŻĘ÷ÖŠ³äČė2molH2”¢2 molCOŗĶ2molSO2·¢Éś·“Ó¦¢Ł”¢¢Ś£¬µŚ5minŹ±“ļµ½Ę½ŗā£¬²āµĆ»ģŗĻĘųĢåÖŠCO2”¢H2O(g)µÄĪļÖŹµÄĮæ·Ö±šĪŖ1.6 mol”¢1.8 mol”£
¢ŁøĆĪĀ¶ČĻĀ£¬·“Ó¦¢ŚµÄĘ½ŗā³£ŹżKĪŖ_____”£
¢ŚĘäĖūĢõ¼ž²»±ä£¬ŌŚµŚ 7 min Ź±ĖõŠ”ČŻĘ÷Ģå»ż£¬SO2µÄĘ½ŗāÅضČ_____(Ģī”°Ōö“ó”±”°¼õŠ””±»ņ”°²»±ä”±)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚ³£ĪĀĻĀ£¬Ļņ![]() ČÜŅŗÖŠÖšµĪ¼ÓČė
ČÜŅŗÖŠÖšµĪ¼ÓČė![]() ČÜŅŗ£¬»ģŗĻČÜŅŗµÄ
ČÜŅŗ£¬»ģŗĻČÜŅŗµÄ![]() ±ä»ÆĒéæöČēĶ¼ÖŠĖłŹ¾ĒśĻߣØĢå»ż±ä»ÆŗöĀŌ²»¼Ę£©”£ĻĀĮŠŠšŹöÕżČ·µÄŹĒ£Ø £©
±ä»ÆĒéæöČēĶ¼ÖŠĖłŹ¾ĒśĻߣØĢå»ż±ä»ÆŗöĀŌ²»¼Ę£©”£ĻĀĮŠŠšŹöÕżČ·µÄŹĒ£Ø £©
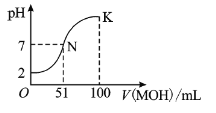
A.![]() ČÜŅŗµÄ
ČÜŅŗµÄ![]() B.
B.![]() µćŹ±¼ÓĖ®Ļ”ŹĶČÜŅŗ£¬
µćŹ±¼ÓĖ®Ļ”ŹĶČÜŅŗ£¬![]() ¼õŠ”
¼õŠ”
C.ŌŚ![]() µć£¬
µć£¬![]() D.ŌŚ
D.ŌŚ![]() µć£¬
µć£¬![]()
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¢ń.»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ĢžAµÄ½į¹¹¼ņŹ½ĪŖ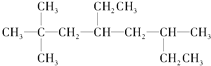 £¬ÓĆĻµĶ³ĆüĆū·ØĆüĆūĢžA£ŗ____________”£
£¬ÓĆĻµĶ³ĆüĆū·ØĆüĆūĢžA£ŗ____________”£
£Ø2£©Ä³ĢžµÄ·Ö×ÓŹ½ĪŖ![]() £¬ŗĖ“Ź²ÕńĒāĘ×Ķ¼ÖŠĻŌŹ¾4øö·å£¬ŌņøĆĢžµÄŅ»ĀČ“śĪļÓŠ_______ÖÖ£¬øĆĢžµÄ½į¹¹¼ņŹ½ĪŖ____________”£
£¬ŗĖ“Ź²ÕńĒāĘ×Ķ¼ÖŠĻŌŹ¾4øö·å£¬ŌņøĆĢžµÄŅ»ĀČ“śĪļÓŠ_______ÖÖ£¬øĆĢžµÄ½į¹¹¼ņŹ½ĪŖ____________”£
£Ø3£©Āé»ĘĖŲÓÖ³Ę»Ę¼ī£¬ŹĒĪŅ¹śĢŲ¶ØÖŠŅ©²ÄĀé»ĘÖŠĖłŗ¬ÓŠµÄŅ»ÖÖÉśĪļ¼ī”£¾æĘѧ¼ŅŃŠ¾æ·¢ĻÖĘä½į¹¹ĪŖ£ŗ £¬ĻĀĮŠø÷ĪļÖŹ£ŗA.
£¬ĻĀĮŠø÷ĪļÖŹ£ŗA. 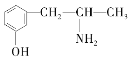 B.
B. ![]() C.
C. 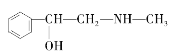 D.
D. 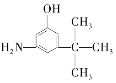 E.
E. 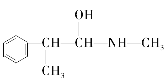
ÓėĀé»ĘĖŲ»„ĪŖĶ¬·ÖŅģ¹¹ĢåµÄŹĒ_________£ØĢī×ÖÄø£¬ĻĀĶ¬£©£¬»„ĪŖĶ¬ĻµĪļµÄŹĒ___________£ØĢī×ÖÄø£©”£
¢ņ.ÓŠ»śĪļC³£ÓĆÓŚŹ³Ę·ŠŠŅµ”£ŅŃÖŖ![]() ŌŚ×ćĮæ
ŌŚ×ćĮæ![]() ÖŠ³ä·ÖČ¼ÉÕ£¬½«Éś³ÉµÄ»ģŗĻĘųĢåŅĄ“ĪĶعż×ćĮæµÄÅØĮņĖįŗĶ¼īŹÆ»Ņ£¬·Ö±šŌöÖŲ
ÖŠ³ä·ÖČ¼ÉÕ£¬½«Éś³ÉµÄ»ģŗĻĘųĢåŅĄ“ĪĶعż×ćĮæµÄÅØĮņĖįŗĶ¼īŹÆ»Ņ£¬·Ö±šŌöÖŲ![]() ŗĶ
ŗĶ![]() £¬¾¼ģŃéŹ£ÓąĘųĢåĪŖ
£¬¾¼ģŃéŹ£ÓąĘųĢåĪŖ![]() ”£
ӣ
£Ø1£©C·Ö×ÓµÄÖŹĘ×Ķ¼ČēĶ¼ĖłŹ¾£¬“ÓĶ¼ÖŠæÉÖŖĘäĻą¶Ō·Ö×ÓÖŹĮæŹĒ________£¬ŌņCµÄ·Ö×ÓŹ½ŹĒ_______”£
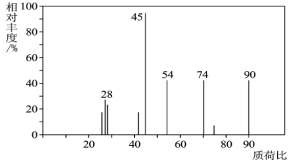
£Ø2£©CÄÜÓė![]() ČÜŅŗ·¢Éś·“Ó¦£¬CŅ»¶Øŗ¬ÓŠµÄ¹ŁÄÜĶÅŹĒ_____________”£
ČÜŅŗ·¢Éś·“Ó¦£¬CŅ»¶Øŗ¬ÓŠµÄ¹ŁÄÜĶÅŹĒ_____________”£
£Ø3£©C·Ö×ÓµÄŗĖ“Ź²ÕńĒāĘ×ÓŠ4øö·å£¬·åĆ껿֮±ČŹĒ![]() £¬ŌņCµÄ½į¹¹¼ņŹ½ŹĒ________”£
£¬ŌņCµÄ½į¹¹¼ņŹ½ŹĒ________”£
£Ø4£©![]() Óė
Óė![]() µÄĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦£¬ŠčČÜŅŗµÄĢå»żŹĒ_____
µÄĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦£¬ŠčČÜŅŗµÄĢå»żŹĒ_____![]() ”£
ӣ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø1£©Ķس£°Ń²šæŖ1 molij»Æѧ¼üĖłĪüŹÕµÄÄÜĮæ擳ÉøĆ»Æѧ¼üµÄ¼üÄÜ”£¼üÄܵēóŠ”æÉŅŌŗāĮæ»Æѧ¼üµÄĒæČõ£¬Ņ²æÉÓĆÓŚ¹ĄĖć»Æѧ·“Ó¦µÄ·“Ó¦ČČ(¦¤H)£¬»Æѧ·“Ó¦µÄ¦¤HµČÓŚ·“Ó¦ÖŠ¶ĻĮŃ¾É»Æѧ¼üµÄ¼üÄÜÖ®ŗĶ¼õČ„·“Ó¦ÖŠŠĪ³ÉŠĀ»Æѧ¼üµÄ¼üÄÜÖ®ŗĶ”£ĻĀĆęĮŠ¾ŁĮĖŅ»Š©»Æѧ¼üµÄ¼üÄÜŹż¾Ż£¬¹©¼ĘĖćŹ¹ÓĆ”£
»Æѧ¼ü | Si”ŖO | Si”ŖCl | H-H | H”ŖCl | Si”ŖSi | Si”ŖC |
¼üÄÜ/kJ”¤mol£1 | 460 | 360 | 436 | 431 | 176 | 347 |
ŅŃÖŖ£ŗ1mol¾§Ģå¹čŗ¬ÓŠ2molSi-Si¼ü”£¹¤ŅµÉĻæÉŅŌĶعżĻĀĮŠ·“Ó¦ÖĘČ”øß“æ¹č£ŗSiCl4(g)£«2H2(g)£½Si(s)£«4HCl(g)£¬ŌņøĆ·“Ó¦µÄ·“Ó¦ČČ(¦¤H)ĪŖ______”£
£Ø2£©Ģ¼ŹĒŠĪ³É»ÆŗĻĪļÖÖĄą×ī¶ąµÄŌŖĖŲ£¬Ę䵄֏¼°»ÆŗĻĪļŹĒČĖĄąÉś²śÉś»īµÄÖ÷ŅŖÄÜŌ“ĪļÖŹ”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
¢ŁÓŠ»śĪļM¾¹żĢ«Ńō¹ā¹āÕÕæÉ×Ŗ»Æ³ÉN£¬×Ŗ»Æ¹ż³ĢČēĻĀ£ŗ
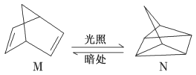 ¦¤H£½£«88.6 kJ”¤mol£1
¦¤H£½£«88.6 kJ”¤mol£1
ŌņMµÄ»ÆѧŹ½ĪŖ_________________£¬M”¢NĻą±Č£¬½ĻĪČ¶ØµÄŹĒ____________”££ØĢīM»ņN£©
¢ŚŅŃÖŖCH3OH(l)µÄČ¼ÉÕČČĪŖ238.6 kJ”¤mol£1£¬CH3OH(l)£«1/2O2(g)=CO2(g)£«2H2(g)””¦¤H£½£a kJ”¤mol£1£¬Ōņa____________238.6(Ģī”°£¾”±”¢”°£¼”±»ņ”°£½”±)”£
¢ŪŹ¹Cl2ŗĶH2O(g)Ķعż×ĘČȵÄĢæ²ć£¬Éś³ÉHClŗĶCO2£¬µ±ÓŠ1 mol Cl2²ĪÓė·“Ó¦Ź±ŹĶ·Å³ö145 kJČČĮ棬Š“³öøĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½£ŗ____________”£
¢Ü»š¼żŗĶµ¼µÆ±ķĆęµÄ±”²ćŹĒÄĶøßĪĀĪļÖŹ”£½«ŹÆÄ«”¢ĀĮ·ŪŗĶ¶žŃõ»ÆīŃ°“Ņ»¶Ø±ČĄż»ģŗĻŌŚøßĪĀĻĀģŃÉÕ£¬ĖłµĆĪļÖŹæÉ×÷ÄĶøßĪĀ²ÄĮĻ£¬4Al(s)£«3TiO2(s)£«3C(s)=2Al2O3(s)£«3TiC(s)””¦¤H£½£1176 kJ”¤mol£1£¬Ōņ·“Ó¦¹ż³ĢÖŠ£¬Ćæ×ŖŅĘ1 molµē×ÓŹ±·Å³öµÄČČĮæĪŖ_______”£
£Ø3£©ŅŃÖŖ£ŗ
¢ŁH2O(g)£½H2O(l) ”÷H1=”ŖQ1kJ/mol
¢ŚCH3OH(g)£½CH3OH(l) ”÷H2=”ŖQ2kJ/mol
¢Ū2CH3OH(g)+3O2(g)£½2CO2(g)+4H2O(g) ”÷H3=”ŖQ3kJ/mol£ØQ1”¢Q2”¢Q3¾ł“óÓŚ0£©
ČōŅŖŹ¹32gŅŗĢ¬¼×“¼ĶźČ«Č¼ÉÕ£¬×īŗó»Öø“µ½ŹŅĪĀ£¬·Å³öµÄČČĮæĪŖ______kJ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓŠ¹ŲĆčŹö¼°»ÆѧÓĆÓļµÄ±ķŹ¾·½·ØÕżČ·µÄŹĒ£Ø £©
A.Ō×ÓŗĖÄŚÓŠ8øöÖŠ×ӵĻłĢ¬Ģ¼Ō×Ó¼Ūµē×ÓÅŲ¼Ķ¼ĪŖ£ŗ![]()
B.NH4FµÄµē×ÓŹ½ĪŖ£ŗ![]() £¬ČżÖÖŌŖĖŲÖŠ·śµÄµŚŅ»µēĄėÄÜ×ī“ó
£¬ČżÖÖŌŖĖŲÖŠ·śµÄµŚŅ»µēĄėÄÜ×ī“ó
C.ĶŹōÓŚdĒųŌŖĖŲ£¬äåŹōÓŚpĒųŌŖĖŲ£¬¶žÕß»łĢ¬Ō×ÓĪ“³É¶Ōµē×ÓŹżÄæĻąĶ¬
D.CO2·Ö×ӵĽį¹¹Ź½ĪŖ£ŗO=C=O£¬Ģ¼µÄŌ×Ó°ė¾¶“óÓŚŃõµÄŌ×Ó°ė¾¶
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com