
| A. | Na+、K+、CO32-、SO42- | B. | Cu2+、SO42-、HCO3-、Na+ | ||
| C. | Cu2+、SO42-、NO3-、Fe3+ | D. | OH-、Na+、Mg2+、SO42- |
分析 酸性溶液中存在大量氢离子,
A.碳酸根离子与氢离子反应;
B.铜离子与碳酸氢根离子发生双水解反应,碳酸氢根离子与氢离子反应;
C.四种离子之间不反应,都不与氢离子反应,能够共存;
D.镁离子、氢离子与氢氧根离子反应.
解答 解:A.CO32-与酸性溶液中的氢离子反应,在溶液中不能大量共存,故A错误;
B.Cu2+、HCO3-之间发生反应,HCO3-与酸性溶液中的氢离子反应,在溶液中不能大量共存,故B错误;
C.Cu2+、SO42-、NO3-、Fe3+之间不反应,都不与氢离子反应,在溶液中能够大量共存,故C正确;
D.OH-与H+、Mg2+之间发生反应,在溶液中不能大量共存,故D错误;
故选C.
点评 本题考查离子共存的正误判断,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;试题侧重对学生基础知识的训练和检验,有利于提高学生灵活运用基础知识解决实际问题的能力.


 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源: 题型:选择题
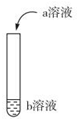 如图进行实验,向试管中的b溶液中加入少量a溶液,试管中现象对应的离子方程式正确的是( ))
如图进行实验,向试管中的b溶液中加入少量a溶液,试管中现象对应的离子方程式正确的是( ))| 选项 | a | b | 试管中现象 | 离子方程式 |
| A | 稀H2SO4 | KI淀粉 | 在空气中放置一段时间后溶液呈黄色 | 4I-+O2+2H2O=2I2+4OH- |
| B | Na2CO3 | 稀盐酸 | 开始时无气泡,后来有气泡 | CO32-+H+=HCO3-; HCO3-+H+=H2O+CO2↑ |
| C | 稀盐酸 | Na2SiO3 | 产生白色胶状物 | 2H++SiO32-=H2SiO3(胶体) |
| D | 稀H2SO4 | 滴有酚酞的Ba(OH)2 | 有白色沉淀生成,溶液由红色变为无色 | Ba2++OH-+H++SO42-= BaSO4↓+H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 青石棉是一种硅酸盐材料 | |
| B. | 青石棉的化学组成可表示为Na2O•3FeO•Fe2O3•8SiO2•H2O | |
| C. | 1 mol青石棉中含有8 mol SiO2 | |
| D. | 1 mol青石棉能还原1 mol HNO3的稀硝酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用CO2合成可降解的聚碳酸酯塑料,可以实现“碳”的循环利用 | |
| B. | 开发利用太阳能、生物质能等清洁能源,有利于节约资源 | |
| C. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| D. | 制备物质时探究化学反应中高的选择性、转化率和原子利用率,属于“绿色”的生产工艺 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MgCO3(s)═MgO(s)+CO2(g)△H=+1.366 kJ/mol | |
| B. | MgCO3(s)═MgO(s)+CO2(g)△H=-1.366 kJ/mol | |
| C. | MgCO3(s)═MgO(s)+CO2(g)△H=-114.7 kJ/mol | |
| D. | MgCO3(s)═MgO(s)+CO2(g)△H=+114.7 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 滴定前 | 第一次终点 | 第二次终点 | 第三次终点 | |
| 滴定管液面刻度 | 0.00mL | 16.02mL | 16.00mL | 16.01mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al14有42个价电子,且与IIA族元素性质相似 | |
| B. | Al13有39个价电子,且与卤素性质类似 | |
| C. | Al13、Al14 互为同素异形体 | |
| D. | Al13原子中存在离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 20mL0.1mol/L CH3COONa溶液与10mL0.1 mol/L HCl溶液混合后溶液呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) | |
| B. | 含等物质的量的NaHC2O4和Na2C2O4的混合溶液:2c(Na +)=3[c(HC2O4-)+c(C2O42-)+c(H2C2O4)] | |
| C. | PH=1的NaH SO4溶液:c(H+)=c(SO42-)+c(OH -) | |
| D. | CO2的水溶液:c(H+)>c(HCO3-)=2c(CO32-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com