
| A. | CuSO4 | B. | HCl | C. | BaCl2 | D. | Na2SO4 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 向含有等物质的量的Ba(OH)2、KOH的混合溶液中通入CO2,与CO2反应的物质依次是:KOH、Ba(OH)2、BaCO3 | |
| B. | 向含有等物质的量的Fe2+、Ag+、Cu2+的混合溶液中加入Zn,与Zn反应的离子依次是:Ag+、Cu2+、Fe2+ | |
| C. | 向含有等物质的量的AlO2-、OH-、CO32-的混合溶液中滴加盐酸,与盐酸反应的物质依次是:AlO2-、Al(OH)3、OH-、CO32- | |
| D. | 在含有等物质的量的FeBr2、FeI2的溶液中,缓慢通入氯气,与氯气反应的离子依次是:I-、Br-、Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 | |
| B. | △H>0表示放热反应,△H<0表示吸热反应 | |
| C. | 在101Kpa时,2g H2完全燃烧生成液态水,放出285.8 KJ热量,氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l)△H=+285.8 kJ•mol-1 | |
| D. | 稀溶液中:H+(aq)+OHˉ(aq)=H2O(l)△H=-53.7 kJ•mol-1,若将含0.5 molH2SO4的浓溶液与含1 molNaOH的溶液混合,放出的热量大于53.7 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
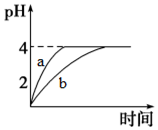 电离平衡、水解平衡、沉淀溶解平衡是溶液中的三大平衡.请回答下列问题:
电离平衡、水解平衡、沉淀溶解平衡是溶液中的三大平衡.请回答下列问题:| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
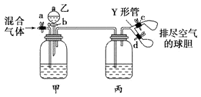 用如图装置来分离CO2和CO混合气体,图中a、c、d为止水夹,b为分液漏斗活塞,通过Y形管和止水夹分别接两个球胆,现装置内空气已排尽,为使实验成功,甲、乙、丙分别盛放的试剂为( )
用如图装置来分离CO2和CO混合气体,图中a、c、d为止水夹,b为分液漏斗活塞,通过Y形管和止水夹分别接两个球胆,现装置内空气已排尽,为使实验成功,甲、乙、丙分别盛放的试剂为( )| 甲 | 乙 | 丙 | |
| A | 饱和NaHCO3溶液 | 12mol•L-1盐酸 | 18.4mol•L-1 H2SO4 |
| B | 饱和Na2CO3溶液 | 2mol•L-1 H2SO4 | 饱和NaOH溶液 |
| C | 饱和NaOH溶液 | 2mol•L-1 H2SO4 | 18.4mol•L-1 H2SO4 |
| D | 18.4mol•L-1 H2SO4 | 饱和NaOH溶液 | 18.4mol•L-1 H2SO4 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
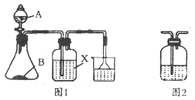 某化学兴趣小组探究二氧化硫和氯气二者的制法和性质,做下列有关实验:
某化学兴趣小组探究二氧化硫和氯气二者的制法和性质,做下列有关实验:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
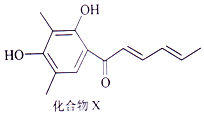 Sorbicillin (简称化合物X)是生产青霉素时的一个副产品,其结构简式如图所示. 下列有关化合物X的说法正确的是( )
Sorbicillin (简称化合物X)是生产青霉素时的一个副产品,其结构简式如图所示. 下列有关化合物X的说法正确的是( )| A. | 分子中所有碳原子可能处于同一平面 | |
| B. | 1 mol化合物X可以与2 mol Na2CO3反应 | |
| C. | 1mol化合物X可以与浓溴水发生取代反应消耗3molBr2 | |
| D. | 化合物X与H2完全加成,每个产物分子中含有4个手性碳原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al2O3$→_{△}^{NaOH(aq)}$NaAlO2(aq)$\stackrel{CO_{2}}{→}$Al(OH)3 | |
| B. | S$\stackrel{O_{2}/点燃}{→}$SO3$\stackrel{H_{2}O}{→}$H2SO4 | |
| C. | N2$\stackrel{O_{2}点燃}{→}$NO2$\stackrel{H_{2}O}{→}$HNO2 | |
| D. | Fe2O3$\stackrel{HCl(aq)}{→}$FeCl3(aq)$\stackrel{△}{→}$无水FeCl3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com