
将浓度为0.1 mol·L-1 HF溶液加水不断稀释,下列各量始终保持增大的是( )
A.c(H+) B.Ka(HF)
C.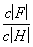 D.
D.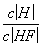
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案科目:高中化学 来源: 题型:
某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
| 实验编号 | 反应物 | 催化剂 |
| ① | 10 mL 2% H2O2溶液 | 无 |
| ② | 10 mL 5% H2O2溶液 | 无 |
| ③ | 10 mL 5% H2O2溶液 | 1 mL 0.1 mol·L-1 FeCl3溶液 |
| ④ | 10 mL 5% H2O2溶液+少量HCl溶液 | 1 mL 0.1 mol·L-1 FeCl3溶液 |
| ⑤ | 10 mL 5% H2O2溶液+少量NaOH溶液 | 1 mL 0.1 mol·L-1 FeCl3溶液 |
(1)催化剂能加快化学反应速率的原因是_________________________________。
(2)常温下5% H2O2溶液的pH约为6,H2O2的电离方程式为___________________________。
(3)实验①和②的目的是___________________________________________。
实验时由于没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进是____________________________。
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如下图:
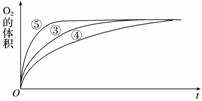
分析上图能够得出的实验结论是____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某化学实验的结果如下表:
| 实验序号 | 反应物 | 在相同温度下测得的反应速率v/mol·L-1·min-1 | |
| 大小相同的金属片 | 酸溶液 | ||
| 1 | 镁条 | 1 mol·L-1盐酸 | v1 |
| 2 | 铁片 | 1 mol·L-1盐酸 | v2 |
| 3 | 铁片 | 0.1 mol·L-1盐酸 | v3 |
下列结论正确的是( )
A.v1>v2>v3 B.v3>v2>v1
C.v1>v3>v2 D.v2>v3>v1
查看答案和解析>>
科目:高中化学 来源: 题型:
按要求回答下列问题。
(1)最新“人工固氮”的研究报道:常温常压、光照条件下,N2在催化剂表面与水发生反应:
2N2(g)+6H2O(l)4NH3(g)+3O2(g)
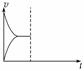
常温下,在恒压密闭容器中上述反应达到平衡后,在其他条件不变时,通入2 mol N2,请在右图中画出正(v正)、逆(v逆)反应速率随时间t变化的示意图。
(2)碳单质在工业上有多种用途。例如焦炭可用来制取水煤气、冶炼金属,活性炭可处理大气污染物NO。
一定条件下,在2 L密闭容器中加入NO和活性炭(无杂质)反应生成气体A和B。当温度在T1 ℃时,测得各物质平衡时物质的量如下表:
| 活性炭(mol) | NO(mol) | A(mol) | B(mol) | |
| 初始 | 2.030 | 0.100 | 0 | 0 |
| 平衡 | 2.000 | 0.040 | 0.030 | 0.030 |
在T1 ℃时,达到平衡共耗时2分钟,则NO的平均反应速率为________ mol·L-1·min-1;当活性炭消耗0.015 mol 时,反应的时间________(填“大于”、“小于”或“等于”)1分钟。
(3)固定和利用CO2,能有效地利用资源,并减少空气中的温室气体。工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:
CO2(g)+3H2(g)CH3OH(g)+H2O(g) ΔH<0
某科学实验小组将6 mol CO2和8 mol H2充入一容积为 2 L 的密闭容器中(温度保持不变),测得H2的物质的量随时间变化如下图中实线所示(图中字母后的数字表示对应的坐标)。回答下列问题:
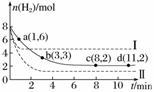
①该反应在0~8 min内CO2的平均反应速率是________ mol·L-1·min-1。
②仅改变某一条件再进行实验,测得H2的物质的量随时间变化如图中虚线所示。与实线相比,曲线 Ⅰ 改变的条件可能是________,曲线 Ⅱ 改变的条件可能是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在Na2CO3中加醋酸产生CO2气体,试从电离平衡常数的角度解释原因[已知:K(CH3COOH)=1.7×10-5;K(H2CO3)=4.3×10-7。]:_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
相同体积、相同pH值的盐酸和醋酸
①加入足量的Zn,在丙图中画出H2体积的变化图像

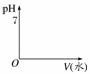
丙 丁
单位时间内,________产生的H2多,反应停止时,______产生的H2多。
查看答案和解析>>
科目:高中化学 来源: 题型:
向等体积等物质的量浓度的H2S和SO2的水溶液中分别通入不同的气体,一段时间后,如图表示通入气体的量与溶液pH关系的曲线图,下列说法中正确的是( )
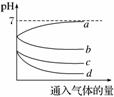
A.曲线a表示向H2S水溶液中通入O2
B.曲线b表示向SO2水溶液中通入O2
C.曲线c表示向H2S水溶液中通入Cl2
D.曲线d表示向SO2水溶液中通入H2S
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.HF、HCl、HBr、HI的熔沸点依次升高
B.H2O的熔点、沸点大于H2S是由于H2O分子之间存在氢键
C.乙醇分子与水分子之间只存在范德华力
D.氯的各种含氧酸的酸性由强到弱排列为HClO>HClO2>HClO3>HClO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com