
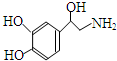
| A. | 去甲肾上腺素分子式C8H10O3N | |
| B. | 每个去甲上腺素分子中含3个碳碳双键、3个酚羟基 | |
| C. | 1mol去甲肾上腺素最多能与2molBr2发生取代反应 | |
| D. | 去甲肾上腺素既能与盐酸反应,又能与氢氧化钠溶液反应 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 叙述I | 叙述II |
| A | 铜丝深入稀硝酸溶液中,溶液变蓝 | 铜丝与硝酸发生了置换反应 |
| B | 浓硫酸具有吸水性和强氧化性 | 把浓硫酸滴到蔗糖表面,蔗糖变黑膨胀 |
| C | Fe3+具有氧化性 | FeCl3溶液用于回收废旧电路板中的Cu |
| D | BaSO4难溶于酸 | 向某溶液加入Ba(NO3)2溶液,再加入足量稀HCl,得到白色沉淀,则原溶液含SO42- |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

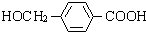 ,I
,I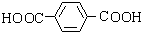 .
. ;C+D→H
;C+D→H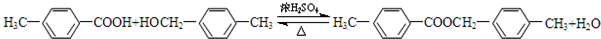 .
.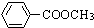 、
、 、
、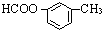
 、
、 ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器内气体密度不再发生变化 | |
| B. | 容器内气体的平均式量不再发生变化 | |
| C. | N2、H2和NH3的物质的量浓度之比为1:3:2 | |
| D. | 单位时间消耗0.1 mol N2的同时生成0.2 mol NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
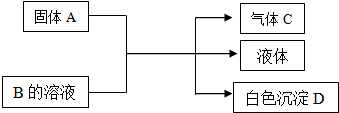
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |
| 原子半径 (10-10m) | 1.52 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 0.71 |
| 最高价态 | +1 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | - |
| 最低价态 | - | - | -2 | - | -4 | -3 | -1 | - | -3 | -1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  和 和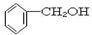 | B. | CH3CH2Cl和CH2ClCH2CH2Cl | ||
| C. | CH3COOH和C17H33COOH | D. | C2H5OH和CH4O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素周期律的本质是原子半径呈周期性变化 | |
| B. | 两种微粒,若核外电子排布完全相同,则其化学性质一定相同 | |
| C. | 阳离子的核外电子排布一定比它的原子少一个电子层 | |
| D. | 两原子如果核外电子排布相同,则一定属于同种元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com