
| A、Na++e--=Na |
| B、2H++4e-=2H2 |
| C、2Cl--2e-=Cl2 |
| D、4OH--4e-=2H2O+O2 |
科目:高中化学 来源: 题型:
| c(OH-) |
| c(H+) |
| A、溶液中水电离出的c(H+)=10-10mol?L-1 |
| B、溶液中c(H+)+c(A-)=0.1 mol?L-1 |
| C、与0.05 mol?L-1NaOH溶液等体积混合后所得溶液中离子浓度大小关系为:c(A-)>c(Na+)>c(OH-)>c(H+) |
| D、上述溶液中加入一定量CH3COONa晶体或加水稀释,溶液c(OH-)均增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.5 mol |
| B、2 mol |
| C、1 mol |
| D、5 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、△H<0,△S>0 |
| B、△H>0,△S>0 |
| C、△H<0,△S<0 |
| D、△H>0,△S<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电化学腐蚀要比化学腐蚀普遍的多,但腐蚀速度要比化学腐蚀慢得多 |
| B、当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用 |
| C、海轮外壳连接锌块是采用牺牲阳极的阴极保护法保护外壳不受腐蚀 |
| D、地下输油钢管与外加直流电源的正极相连可保护其不受腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
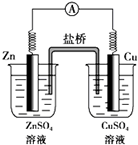
| A、反应中,盐桥中的Cl-会移向ZnSO4溶液 |
| B、取出盐桥后,电流计依然发生偏转 |
| C、铜片上有气泡逸出 |
| D、锌为负极,发生还原反应,电极反应式为:Zn-2e-=Zn2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
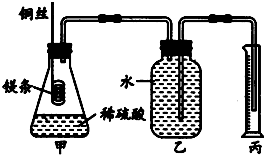 化学兴趣小组设计测定镁原子的摩尔质量的实验,简易装置如图,除去表面氧化膜的镁条质量为0.24g,镁条完全反应后,用量筒收集水,体积为0.224L(设已折换成标准状况下的对应的气体体积).
化学兴趣小组设计测定镁原子的摩尔质量的实验,简易装置如图,除去表面氧化膜的镁条质量为0.24g,镁条完全反应后,用量筒收集水,体积为0.224L(设已折换成标准状况下的对应的气体体积).查看答案和解析>>
科目:高中化学 来源: 题型:
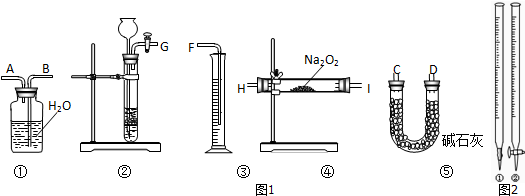
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com