
【题目】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为,下列叙述不正确的是
3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH
A.放电时每转移3mol电子,正极有1molK2FeO4被氧化
B.充电时阳极反应为:Fe(OH)3—3e—+5OH—=FeO42-+4H2O
C.放电时负极反应为:Zn—2e—+2OH—=Zn(OH)2
D.放电时正极附近溶液的碱性增强
 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】正硼酸(H3BO3)是一种层状结构白色晶体,层内的H3BO3分子通过氢键相连(如图)。下列有关说法正确的是
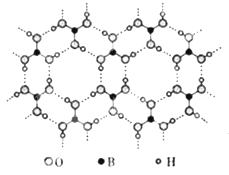
A.正硼酸晶体属于分子晶体
B.分子中硼原子最外层为8e-稳定结构
C.H3BO3分子的稳定性与氢键有关
D.含1mol H3BO3的晶体中有6mol氢键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为2L的密闭容器中发生反应xA(g)+yB(g)![]() zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是( )
zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是( )

A. 200℃时,反应从开始到平衡的平均速率v(B)=0.04 mol·L-1·min-1
B. 200℃时,该反应的平衡常数为25
C. 当外界条件由200℃降温到100℃,原平衡一定被破坏,且正逆反应速率均增大
D. 由图乙可知,反应xA(g)+yB(g)![]() zC(g)的ΔH<0,且a=2
zC(g)的ΔH<0,且a=2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某二元酸(化学式用H2B表示)在水中的电离方程式:H2B=H++HB-,HB-![]() H++B2-。回答下列问题:
H++B2-。回答下列问题:
(1) NaHB溶液显 (填“酸性”“中性”或“碱性”)。理由是 。
(2)在0.1 mol·L-1的Na2B溶液中,下列粒子浓度关系式正确的是 。
A.c(B2-)+c(HB-)+c(H2B)=0.1 mol·L-1
B.c(OH-)=c(H+)+c(HB-)
C.c(Na+)+c(H+)=c(OH-)+c(HB-)+2c(B2-)
D.c(Na+)=2c(B2-)+2c(HB-)
(3)0.1 mol·L-1 Na2B溶液中各种离子浓度由大到小的顺序是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,如果取0.1 mol·L-1 HA溶液与0.1 mol·L-1 NaOH溶液等体积混合(混合后溶液体积的变化不计),测得混合溶液的pH=8,试回答以下问题:
(1)混合溶液的pH=8的原因(用离子方程式表示): ;
(2)混合溶液中由水电离出的c(H+) (填 “<”“>”或“=”)0.1 mol·L-1 NaOH溶液中由水电离出的c(H+);
(3)已知NH4A溶液为中性,又知将HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH (填“<”“>”或“=”)7;
(4)将相同温度下相同浓度的五种溶液:①(NH4)2CO3 ②NH3·H2O ③(NH4)2SO4 ④NH4Cl ⑤CH3COONH4;按c(NH4+)由大到小的顺序排列 (填序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将50g密度ρ=0.98g/mL的10%的氨水和100g密度ρ=0.93g/mL的40%的氨水混合,得到ρ=0.95g/mL氨水溶液,求所得氨水的物质的量浓度是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2016北京】以废旧铅酸电池中的含铅废料(Pb、PbO、PbO2、PbSO4及炭黑等)和H2SO4为原料,制备高纯PbO,实现铅的再生利用。其工作流程如下:
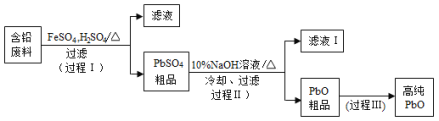
(1)过程Ⅰ中,在Fe2+催化下,Pb和PbO2反应生成PbSO4的化学方程式是__________。
(2)过程Ⅰ中,Fe2+催化过程可表示为:
i:2Fe2++ PbO2+4H++SO42=2Fe3++PbSO4+2H2O
ii: ……
① 写出ii的离子方程式:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】选择下列实验方法分离物质,将分离方法的代号填在括号里.A.萃取分液 B.过滤 C.分液 D.蒸馏
①从碘水中分离出碘.
②分离水和汽油的混合物.
③分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物. .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com