
 发散思维新课堂系列答案
发散思维新课堂系列答案科目:高中化学 来源: 题型:


| 水 |
| 水 |

 +CH3CH2Cl
+CH3CH2Cl +HCl
+HCl +CH3CH2Cl
+CH3CH2Cl +HCl
+HCl

查看答案和解析>>
科目:高中化学 来源: 题型:

| ||
| 红磷(少许) |

| Cl2 |
| 红磷(少许) |
| C |
| (Mt=150.5) |




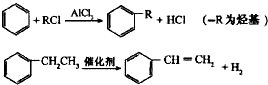
 +RCl
+RCl| 催化剂 |
 (-R为羟基)
(-R为羟基)
| 催化剂 |
 (-R为羟基)
(-R为羟基)



查看答案和解析>>
科目:高中化学 来源: 题型:


 +CH3CH2Cl
+CH3CH2Cl +HCl
+HCl +CH3CH2Cl
+CH3CH2Cl +HCl
+HCl

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:
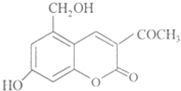 有机物X是亮菌甲素注射液的有效成分,结构简式如图所示.下列关于X的判断正确的是( )
有机物X是亮菌甲素注射液的有效成分,结构简式如图所示.下列关于X的判断正确的是( )| A、有机物X中含有5种含氧官能团,遇FeCl3溶液显紫色 | B、有机物X是芳香烃的衍生物,且含有2个苯环 | C、1mol有机物X最多能与5molH2发生加成反应 | D、1mol有机物X在一定条件下与NaOH溶液反应,最多能消耗2molNaOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com