
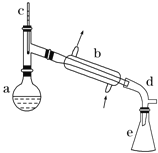
【题目】醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下:

可能用到的有关数据如下:
相对分子质量 | 密度/(g/cm3) | 沸点/℃ | 溶解性 | |
环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
合成反应:
在a中加入20g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1mL浓H2SO4 。b中通入冷却水后,开始缓慢加热a,控制馏出物温度不超过90℃。
分离提纯:
反应粗产物倒入分流漏斗中,分别利用少量5%碳酸钠溶液和水洗涤,分离后加入无水CaCl2颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得纯净环己烯10g。
回答下列问题:
(1)装置b的名称是_____。
(2)加入碎瓷片的作用是_____,如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是_______(填正确答案标号)。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)本实验中最容易产生副产物的结构简式为_______。
(4)分液漏斗在使用前须清洗干净并________,在实验分离过程中产物应该从分液漏斗的________(填“上口倒出”或“下口放出”)。
(5)分离提纯过程中加入无水氯化钙的目的是_____。
(6)在环己烯粗产物蒸馏过程中,不可能用到的仪器有________(填正确答案标号)。
A.圆底烧瓶 B.温度计 C.吸滤瓶 D.球形冷凝管 E.接收器
(7)本实验中所得的环己烯的产率是________ (填正确答案的标号)。
A.41% B.50% C.61% D.70%
【答案】直形冷凝管 防止暴沸B![]() 检漏上口倒出干燥(或除水除醇)C DC
检漏上口倒出干燥(或除水除醇)C DC
【解析】
(1)由实验装置图可以识别b装置是直型冷凝管,是蒸馏冷凝的基本实验仪器。
(2)碎瓷片因为表面有很多小孔,在实验溶液加热操作中用来防止暴沸,碎瓷片应该在溶液加热前加入,如果忘记加入,为了安全起见,也应该将溶液冷却后再行加入。
(3)本实验的反应是醇在浓硫酸催化加热的条件下发生分子内脱水而生成烯,但是也应当注意到,在相同的条件下醇同样可以发生分子间的脱水反应而生成醚。故环己醇的脱水可生成副产物环己醚,结构简式为:![]() 。
。
(4)分液漏斗操作前检漏是必要操作步骤,由题干所给的性质表格可以发现环己烯的密度小于环己醇,故环己烯应该在上层,从上口倒出。
(5)分离提纯时“无水”氯化钙是作为干燥剂,可以除去产物中混有的少量的醇和水,一般无水试剂在实验中都是作为干燥剂。
(6)蒸馏过程要用到的仪器主要有:圆底烧瓶、温度计、酒精灯、直形冷凝管、铁架台、接收器(锥形瓶)、接引管(牛角管)等。故应该选CD。
(7)原反应物环己醇质量20克,根据反应式可知理论生成环己烯质量为![]() ,实际生成环己烯10g,故产率为61%,故选C。
,实际生成环己烯10g,故产率为61%,故选C。


 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】对于可逆反应:2SO2(g)+O2(g)![]() 2SO3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是( )
2SO3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是( )
A. 增大压强 B. 升高温度 C. 使用催化剂 D. 多充O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项叙述中,正确的是( )
A. Si、P、S的第一电离能随原子序数的增大而增大
B. 价电子排布为3d64s2的元素位于第四周期第ⅧB族,是d区元素
C. 2p和3p轨道形状均为哑铃形,能量不相等
D. 氮原子的最外层电子排布图:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羰基硫(COS)是全球硫循环的重要中间体,也是有机合成中的重要原料,是化学工作者重要的研究对象。已知:
Ⅰ.COS(g)+H2(g)![]() H2S(g)+CO(g) △Hl=-17kJ/mol;
H2S(g)+CO(g) △Hl=-17kJ/mol;
Ⅱ.COS(g)+H2O(g)![]() H2S(g)+CO2(g) △H2=-35kJ/mol。
H2S(g)+CO2(g) △H2=-35kJ/mol。
回答下列问题:
(1)反应CO(g)+H2O(g)![]() H2(g)+CO2(g)的△H=________。
H2(g)+CO2(g)的△H=________。
(2)在充有催化剂的恒压密闭容器中进行反应I。设起始充入的n(H2):n(COS)=m,相同时间内测得COS转化率与m和温度(T)的关系如图所示。
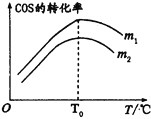 ①m1________m2(填>、<或=)。
①m1________m2(填>、<或=)。
②温度高于T0时,COS转化率减小的可能原因为_________。
A.有副反应发生。
B.反应的△H增大。
C.催化剂活性降低。
D.逆反应速率增大的倍数小于正反应速率增大的倍数
(3)在恒温、恒容密闭容器中.进行反应I。下列说法中能说明反应I已达到平衡状态的是___________。
A.c(H2S)=c(CO) B.v正(H2)=v逆(H2S)
C.容器中气体密度保持不变 D.容器中混合气体平均摩尔质量保持不变
E.c(COS)保持不变
(4)某温度下,向体积为2 L的恒容密闭容器中通入5 mol COS(g)和5 molH2O(g),发生反应Ⅱ,5 min后反应达到平衡,测得COS(g)的转化率为80%。
①反应从起始至5 min内,用H2S浓度变化表示的平均反应速度v(H2S)=________。
②该温度下,上述反应的平衡常数K=________。
③其他条件相同时,既能使上述反应中COS的平衡转化率降低,又能使反应速率加快的做法是________。
A.缩小容器容积 B.升高温度
C.分离出硫化氢 D.加入一定量H2O(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验小组用下列装置进行乙醇催化氧化的实验。已知:乙醛可被氧化为乙酸。
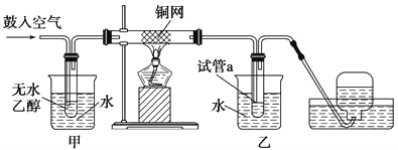
(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式__________________ 、_____________________。
(2)在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇催化反应是____________ 反应。进一步研究表明,鼓入空气的速率与反应体系的温度关系曲线如图所示。
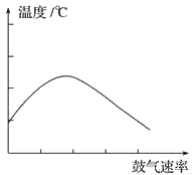
试解释出现图中现象的原因_______________________。
(3)甲和乙两个水浴作用不相同。甲的作用是_______________;乙的作用是______________。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有_______。要除去该物质,可在混合液中加入________ (填写字母)。然后,再通过________________(填实验操作名称)即可除去。
A.氯化钠溶液 B.苯 C.碳酸氢钠溶液 D.四氯化碳
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com