
 麻黄素又称黄碱,是我国特定的中药材麻黄中所含的一种生物碱.经我国科学工作者研究发现其结构如图:
麻黄素又称黄碱,是我国特定的中药材麻黄中所含的一种生物碱.经我国科学工作者研究发现其结构如图: 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
| 化学键 | A-A | B-B | A-B |
| 生成1mol化学键时放出的能量 | 436kJ?mol-1 | 243kJ?mol-1 | 431kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 3 |
| 2 |
| 1 |
| 2 |
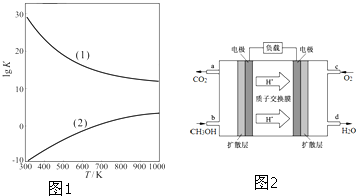
查看答案和解析>>
科目:高中化学 来源: 题型:
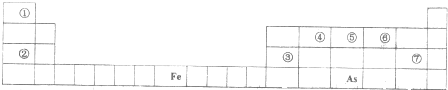
查看答案和解析>>
科目:高中化学 来源: 题型:
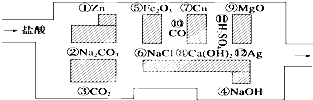
查看答案和解析>>
科目:高中化学 来源: 题型:
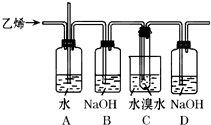 已知1,2-二溴乙烷的主要物理性质如表:
已知1,2-二溴乙烷的主要物理性质如表:| 熔点 | 沸点 | 密度 | 溶解性 |
| 9.79°C | 131.4°C | 2.18g/cm3 | 难溶于水,易溶于醇、醚等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验次数 | 起始温度t1/℃ | 终止温度 t2/℃ | |
| 盐酸 | NaOH | ||
| 1 | 20.2 | 20.3 | 23.7 |
| 2 | 20.3 | 20.5 | 23.8 |
| 3 | 21.5 | 21.6 | 24.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、醋酸不小心滴到大理石桌面上,桌面失去光泽 |
| B、熏醋可一定程度上防止流行性感冒 |
| C、醋可以除去水壶上的水垢 |
| D、用醋烹饪鱼,除去鱼的腥味 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com