
| A. | 8种 | B. | 9种 | C. | 10种 | D. | 11种 |
分析 先分别讨论①-X、-Y、-Z都相邻,②-X、-Y、-Z都不相邻③-X、-Y、-Z只有两种相邻时含有的同分异构体,然后计算出该有机物总共含有的同分异构体数目.
解答 解:①-X、-Y、-Z都相邻的情况:三种取代基分别在中间时存在的结构不同,所以总共有3种同分异构体;
②-X、-Y、-Z都不相邻:三种取代基都在苯环的间位氢原子位置,只有1种结构;
③-X、-Y、-Z中只有两个相邻:羟基、羧基和甲基相邻的取代基有3种组合,剩余的取代基有2种间位取代,所以取代产物有:3×2=6种;
所以总共含有的同分异构体数目为:3+1+6=10.
故选:C.
点评 本题考查了同分异构体的求算,题目难度中等,注意掌握同分异构体的概念及求算方法,在求算同分异构体时,必须避免重复的结构,如:-X、-Y、-Z都相邻时,含有3种同分异构体,不是6种.


 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 石油是混合物,其分馏产品汽油为纯净物 | |
| B. |  的核磁共振氢谱中有4种峰 的核磁共振氢谱中有4种峰 | |
| C. | 苯甲酸的重结晶实验中,粗苯甲酸溶解后还要加点水的目的是减少过滤时苯甲酸的损失 | |
| D. | 苯中滴加浓溴水,充分震荡后溴水层褪色,是因为苯与溴水中的溴发生了加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
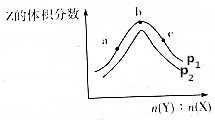 一定温度下,某密闭容器中存在反应:X(g)+2Y(g)?2Z(g),测得平衡体系中Z的体积分数与体系的压强(p)、投料比[b(Y):n(X)]关系如图所示,下列分析一定正确的是( )
一定温度下,某密闭容器中存在反应:X(g)+2Y(g)?2Z(g),测得平衡体系中Z的体积分数与体系的压强(p)、投料比[b(Y):n(X)]关系如图所示,下列分析一定正确的是( )| A. | p2>p1 | B. | Y的转化率:a<c<b | ||
| C. | b点时n(Y):n(X)=2 | D. | 该反应是一个放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 组别 | 草酸的体积(mL) | 温度 | 其他物质 |
| ① | 2Ml | 20 | 无 |
| ② | 2mL | 20 | 10滴饱和MnS04溶液 |
| ③ | 2mL | 30 | 无 |
| ④ | 1mL | 20 | 1mL蒸馈水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 向某溶液中加入足量稀盐酸无现象,再滴加BaCl2溶液 | 有白色沉淀生成 | 原溶液中有SO42- |
| B | Agl沉淀中滴入稀KCl溶液 | 有白色沉淀生成 | AgCl比AgI更难溶 |
| C | 向CH3CH2X中加入少量AgNO3溶液,加热 | 有浅黄色沉淀生成 | CH3CH2X中含有Br- |
| D | C2H5OH与浓硫酸170℃共热,制得的气体通入酸性KMnO4溶液 | KMnO4溶液褪色 | 使KMnO4溶液褪色的是乙烯 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
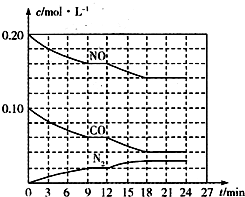 为有效控制雾霾,各地积极采取措施改善大气质量.有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要.
为有效控制雾霾,各地积极采取措施改善大气质量.有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要.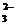 )+c(HSO
)+c(HSO )(用含硫微粒浓度的代数式表示).
)(用含硫微粒浓度的代数式表示).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com