
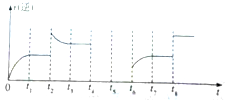
 ú��������úΪԭ�ϣ�������ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ���̣�
ú��������úΪԭ�ϣ�������ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ���̣�| ʵ �� �� | �� �� /�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
| H2O��g�� | CO | H2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
| ||
| ��t |
| ||
| ��t |
| ||
| 5min |
| 4mol-2.4mol |
| 4mol |
| 2mol-1.6mol |
| 2mol |
 ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���������ⸯʴ |
| B����������������������Ӧ |
| C������1.12g���۵����������������������������336mL����״���� |
| D���������ȣ��Ӷ������¶ȣ����ʸ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
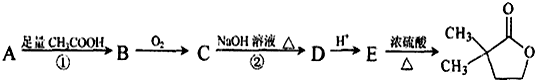
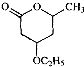 ��B��һ����Ҫ��ͬ���칹�壮����ƺ�����������ɴ�
��B��һ����Ҫ��ͬ���칹�壮����ƺ�����������ɴ�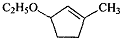 ��
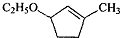
��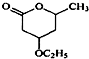 �ĺϳ�·�ߣ�������ͼ��ʾ����ע����Ӧ��������
�ĺϳ�·�ߣ�������ͼ��ʾ����ע����Ӧ��������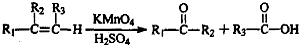 ��
��| Ũ���� |
| 170�� |
| ���¡���ѹ |
| ���� |
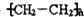 ��
��
| H2O |
| ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���¸�ѹ |
| ���� |
 B��
B�� C��
C�� D��
D��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������һ�����ʵ���Ũ�ȵ���Һ���õ�����ƿ |
| B���ռ�����Ȫʵ�����õ�Բ����ƿ |
| C���к͵ζ�ʵ���е���ʽ�ζ��� |
| D���к͵ζ�ʵ���е���ƿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��AgCl+2NH3?H2O��[Ag��NH3��2]Cl+2H2O |
| B��CuSO4+H2S��CuS��+H2SO4 |
| C��KCl��l��+Na��l����K��+NaCl��l�� |
| D��2[Ag��NH3��2]Cl+Na2S��Ag2S��+2NaCl+4NH3 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com