
分析 根据电解质、非电解质的定义分析,电解质是在熔融状态或水溶液中能导电的化合物,非电解质是在熔融状态和水溶液中都不导电的化合物,单质、混合物既不是电解质也不是非电解质,
强电解质是指在水溶液中能完全电离的电解质,
弱电解质是指在水溶液中不能完全电离的电解质.
解答 解:强电解质是指在水溶液中能完全电离的电解质,包括强酸、强碱和大多数盐,①NaCl、②NaOH、③H2SO4 、属于强电解质,
弱电解质是指在水溶液中不能完全电离的电解质,包括弱酸、弱碱,、⑤CH3COOH、⑥NH3•H2O、⑩水,
非电解质是在熔融状态和水溶液中都不导电的化合物,⑧乙醇、⑨蔗糖的水溶液不导电,属于非电解质,
故答案为:①②③;⑤⑥⑩;⑧⑨.
点评 本题考查电解质、非电解质、强电解质和如电解质的概念和分类,题目难度不大,注意基础知识的积累.


科目:高中化学 来源: 题型:选择题
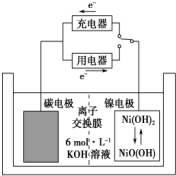 一种碳纳米管能够吸附氢气,可作二次电池(如图所示)的碳电极.该电池的电解质溶液为6mol•L-1的KOH溶液,下列说法中不正确的是( )
一种碳纳米管能够吸附氢气,可作二次电池(如图所示)的碳电极.该电池的电解质溶液为6mol•L-1的KOH溶液,下列说法中不正确的是( )| A. | 充电时阴极反应:2H2O+2e-═2OH-+H2↑ | |
| B. | 充电时将碳电极与电源的负极相连 | |
| C. | 放电时,OH-移向碳电极 | |
| D. | 放电时镍电极反应为:Ni(OH)2+OH--e-═NiO(OH)+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,0.1 mol•L-1 HA溶液的pH=3,则HA的电离:HA=H++A- | |
| B. | 向硫酸铵溶液中加入适量氨水,当溶液呈酸性时,溶液中c(SO42-)=c(NH4+) | |
| C. | 向1 mL 2 mol•L-1NaOH溶液中滴加1~2滴0.1 mol•L-1MgCl2溶液后,再滴加2滴0.1 mol•L-1 FeCl3溶液:Mg2++2OH-=Mg(OH)2↓,3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+ | |
| D. | 浓度相等的①NH4HSO4②NH4C1③(NH4)2SO4溶液中,c(NH4+)的大小顺序为③>①>② |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
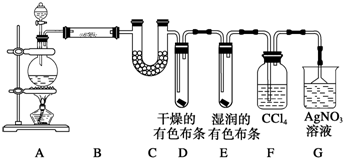 某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题.
某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸钡不溶于水,所以硫酸钡是非电解质 | |
| B. | 二氧化碳溶于水可以导电,所以,二氧化碳是电解质 | |
| C. | 固态磷酸是电解质,所以磷酸在熔化时或溶于水时都能导电 | |
| D. | 液态氯化氢不能导电,但氯化氢是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液 | |
| B. | 往Fe(OH)3胶体中逐滴加入稀H2SO4时,开始时会出现沉淀,再继续滴加时,沉淀又会消失 | |
| C. | Fe(OH)3胶体粒子在电场影响下将向阴极运动,说明Fe(OH)3胶体带正电 | |
| D. | 分离胶体和某盐溶液,可用过滤的方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ①②③ | C. | ①④⑤ | D. | ①②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
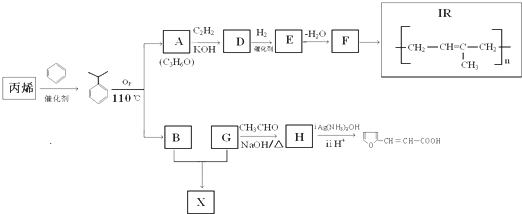
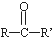 $\stackrel{KOH}{→}$
$\stackrel{KOH}{→}$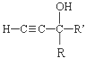
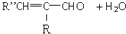 +H2O(-R、-R′、-R″表示可能相同或可能不同的原子或原子团)
+H2O(-R、-R′、-R″表示可能相同或可能不同的原子或原子团) ,反应类型是加成反应.
,反应类型是加成反应. .
. .
. .
.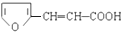 ,符合下列要求的有12种.
,符合下列要求的有12种.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com