
| A、氯气通入水中:Cl2+H2O=H++Cl-+HClO |
| B、石灰石溶于醋酸:CaCO3+2H+=Ca2++CO2↑+H2O |
| C、向Ba(OH)2 溶液中逐滴加入NaHSO4稀溶液至刚好沉淀完全:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| D、钠和冷水反应:Na+2H2O=Na++2OH-+H2↑ |


科目:高中化学 来源: 题型:
| A、原气体中肯定有SO2 |
| B、原气体中肯定没有H2S和HBr |
| C、原气体中肯定有SO2和HCl |
| D、原气体中肯定没有CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K是银白色金属,硬度大,熔点高 |
| B、K在空气可以被空气中的氧气所氧化,且产物只有K2O |
| C、K的活泼性强,所以钾应该保存在水中 |
| D、K与水能够反应,且比Na与水的反应剧烈,产物都有氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、WZ2分子中所有原子最外层都为8电子结构 |
| B、原子半径大小顺序为X<W<Y<Z |
| C、WX2、ZX2水溶液呈酸性,都能导致酸雨 |
| D、WX2是以极性键结合成的非极性分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、M:0.016mol/L |
| B、N:0.02mol/L |
| C、P:0.016mol/L |
| D、Q:0.024mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
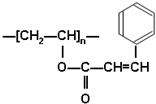 感光高分子材料是制作大规模集成电路不可缺少的材料,感光高分子在曝光时会发生二聚反应,生成不溶性的交联高分子硬化膜,未感光部分可用溶剂或其它药品洗去.常用的感光高分子有聚肉桂酸乙烯酯,它的结构简式如右图,它感光后形成二聚交联高分子.请据此回答下列问题:
感光高分子材料是制作大规模集成电路不可缺少的材料,感光高分子在曝光时会发生二聚反应,生成不溶性的交联高分子硬化膜,未感光部分可用溶剂或其它药品洗去.常用的感光高分子有聚肉桂酸乙烯酯,它的结构简式如右图,它感光后形成二聚交联高分子.请据此回答下列问题: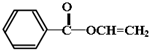 和
和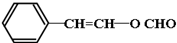 外还有两种,请写出其结构简式:
外还有两种,请写出其结构简式:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com