
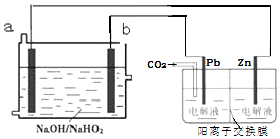
| A. | a为电源的负极 | |
| B. | 阴极的电极反应式为2CO2+2e-═C2O42- | |
| C. | 电解过程中电子的流向为b→Pb→Zn→a | |
| D. | a电极每消耗1mol HO2-,同时可制得0.5molZnC2O4 |
分析 以Al-H2O2燃料电池为电源,采用电化学法还原CO2,制备ZnC2O4,由图可知,a应为正极,Zn为阳极,则Zn失去电子,b为负极,pb为阴极,电子在外电路由负极流向正向,电子不能进入溶液中,结合电子守恒来解答.
解答 解:A.制备ZnC2O4,可知Zn失去电子,则Zn为阳极,Zn与a相连,则a为原电池的正极,故A错误;
B.Pb电极CO2得电子被还原,为阴极,阴极反应为2CO2+2e-═C2O42-,故B正确;
C.电子不能从溶液中通过,所以Pb→Zn错误,故C错误;
D.a电极反应式为HO2-+2e-+H2O═3OH-,由电子守恒可知HO2-~2e-~C2O42-~ZnC2O4,消耗1mol HO2-,转移2mol电子同时可制得1molZnC2O4,故D错误;
故选B.
点评 本题考查原电池和电解池,为高频考点,把握习题中的信息、电极反应判断、电子的移动为解答的关键,侧重分析与应用能力的考查,注意选项D为解答的难点,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题

| A. | 甲的二氯代物有两种 | |
| B. | 乙的结构简式是CH2CH2 | |
| C. | 乙和丙分子中所有原子处于同一个平面上 | |
| D. | 丙分子中存在三个交替出现的碳碳双键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl的水溶液呈强酸性,HF的水溶液也呈强酸性 | |
| B. | CH4是正四面体结构,SiH4也是正四面体结构 | |
| C. | Cl2与Fe反应生成FeCl3,S与Fe反应生成Fe2S3 | |
| D. | CaCO3与稀硝酸反应生成CO2,CaSO3与稀硝酸反应生成SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 其原子半径由大到小顺序为EDCBA | |
| B. | 某物质的焰色反应为黄色,则该物质一定为含D的盐 | |
| C. | 由A、D两种元素形成的化合物中只含有离子键 | |
| D. | 最高价氧化物对应水化物碱性强弱:B>D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,对此高聚物叙述不正确的是( )
,对此高聚物叙述不正确的是( )| A. | 化学式为(C11H10O2)n | |
| B. | 可以发生水解反应、氧化反应,也能发生卤代反应 | |
| C. | 1mol该有机物分子最多能和4molH2发生加成反应 | |
| D. | 该高分子材料是经加聚反应而得到 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它是由Te、Zn、Cd按一定比例混合而成的,无固定的溶沸点 | |
| B. | 它易导电、导热,具有延展性 | |
| C. | 它的熔、沸点比Zn的低 | |
| D. | 它的硬度和强度比Cd的大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某有机物的结构简式如图.1mol该有机物分别与足量的Na、NaOH、NaHCO3反应时,消耗三种物质的物质的量之比为( )
某有机物的结构简式如图.1mol该有机物分别与足量的Na、NaOH、NaHCO3反应时,消耗三种物质的物质的量之比为( )| A. | 3:1:1 | B. | 3:2:1 | C. | 1:1:1 | D. | 3:2:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应中Na2O2既是氧化剂又是还原剂 | |
| B. | Fe2O3可以通过铁丝在氧气中燃烧制得 | |
| C. | 生成1 mol Na2FeO4,有3mol电子转移 | |
| D. | 在Na2FeO4中Fe为+4价,具有强氧化性,能消毒杀菌 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com