
����Ŀ��������G��һ���л��������м��塣��A�Ʊ�G��һ�ֺϳ�·�����£�
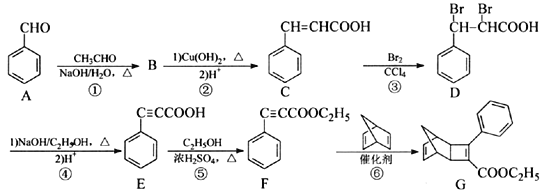
�ش��������⣺
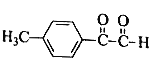
(1)F�еĹ���������Ϊ______��
(2)B�ķ���ʽΪC9H8O��д��B�Ľṹ��ʽ��______��
(3)��Ӧ��~��������ȡ����Ӧ����______(�����)��
(4)д��ͬʱ��������������C��һ��ͬ���칹��Ľṹ��ʽ��______��
���ܷ���������Ӧ�� �����к��б�������4�ֲ�ͬ��ѧ�������⡣
(5)��д����![]() ��CH3C��CHΪԭ���Ʊ�
��CH3C��CHΪԭ���Ʊ�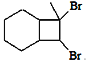 �ĺϳ�·������ͼ(���Լ����ã��ϳ�·������ͼʾ�����������)______��
�ĺϳ�·������ͼ(���Լ����ã��ϳ�·������ͼʾ�����������)______��
���𰸡�������̼̼���� ![]() ��
�� 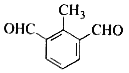 ��
��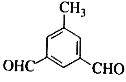 ��
��
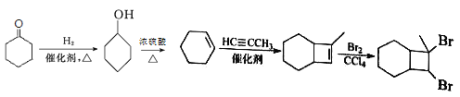
��������
�����л���C��֪���������л���B��������ͭ������Һ����ΪC������BΪȩ�������л���C�Ľṹ���л���A�Ľṹ��ʽ��֪���л���BΪ![]() ���л���C���巢���ӳɷ�Ӧ�����л���D���ṹ��ʽΪ
���л���C���巢���ӳɷ�Ӧ�����л���D���ṹ��ʽΪ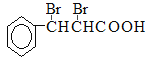 ��D���������Ƶ��Ҵ���Һ�м��ȷ�����ȥ��Ӧ���������ữ��õ��л���E���ṹ��ʽΪ
��D���������Ƶ��Ҵ���Һ�м��ȷ�����ȥ��Ӧ���������ữ��õ��л���E���ṹ��ʽΪ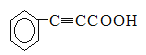 ���л���E���Ҵ���Ũ���������������·���������Ӧ�����л���F���ṹ��ʽΪ
���л���E���Ҵ���Ũ���������������·���������Ӧ�����л���F���ṹ��ʽΪ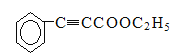 ��F��
��F��![]() �����ӳɷ�Ӧ�����л���G,�ṹ��ʽΪ
�����ӳɷ�Ӧ�����л���G,�ṹ��ʽΪ �������Ϸ������
�������Ϸ������
�����л���C��֪���������л���B��������ͭ������Һ����ΪC������BΪȩ�������л���C�Ľṹ���л���A�Ľṹ��ʽ��֪���л���BΪ![]() ���л���C���巢���ӳɷ�Ӧ�����л���D���ṹ��ʽΪ
���л���C���巢���ӳɷ�Ӧ�����л���D���ṹ��ʽΪ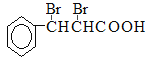 ��D���������Ƶ��Ҵ���Һ�м��ȷ�����ȥ��Ӧ���������ữ��õ��л���E���ṹ��ʽΪ
��D���������Ƶ��Ҵ���Һ�м��ȷ�����ȥ��Ӧ���������ữ��õ��л���E���ṹ��ʽΪ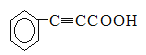 ���л���E���Ҵ���Ũ���������������·���������Ӧ�����л���F���ṹ��ʽΪ
���л���E���Ҵ���Ũ���������������·���������Ӧ�����л���F���ṹ��ʽΪ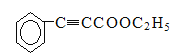 ��F��
��F��![]() �����ӳɷ�Ӧ�����л���G,�ṹ��ʽΪ
�����ӳɷ�Ӧ�����л���G,�ṹ��ʽΪ ��
��
(1)������Ϸ�����֪��F�Ľṹ��ʽΪ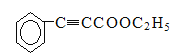 ��F�еĹ���������Ϊ������̼̼������
��F�еĹ���������Ϊ������̼̼������
����������������ǣ�������̼̼������
(2)������Ϸ�����֪��B�ķ���ʽΪC9H8O���л���BΪ![]() ��
��
����������������ǣ�![]() ��
��
(3)������Ϸ�����֪����Ӧ��Ϊ������Ӧ����Ӧ��Ϊ�ӳɷ�Ӧ����Ӧ��Ϊ��ȥ��Ӧ����Ӧ��Ϊ������Ӧ��ȡ����Ӧ������Ӧ��Ϊ�ӳɷ�Ӧ�����Է�Ӧ��~��������ȡ����Ӧ���ǣ��ݣ�
����������������ǣ��ݡ�
(4)�л���C�Ľṹ��ʽΪ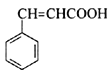 ��C��һ��ͬ���칹�������������������ܷ���������Ӧ������ȩ���������к��б�������4�ֲ�ͬ��ѧ�������⣬������ܵĽṹ�У�
��C��һ��ͬ���칹�������������������ܷ���������Ӧ������ȩ���������к��б�������4�ֲ�ͬ��ѧ�������⣬������ܵĽṹ�У�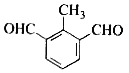 ��
��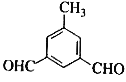 ��
��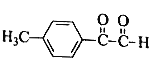 �ȵȣ�������д����һ�֡�
�ȵȣ�������д����һ�֡�
����������������ǣ� ��
�� ��
�� ��
��
(5) ![]() �����������ӳ����ɻ���������������Ũ������������·�����ȥ��Ӧ���ɻ���ϩ������ϩ���Ȳ�����ӳ�����
�����������ӳ����ɻ���������������Ũ������������·�����ȥ��Ӧ���ɻ���ϩ������ϩ���Ȳ�����ӳ�����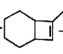 �����������巢���ӳɵõ�Ŀ�����
�����������巢���ӳɵõ�Ŀ�����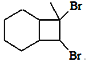 ����������������
����������������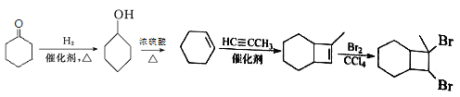 ��
��
����������������ǣ� ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������˵����ȷ���ǣ�������
A. �����£�0.2 mol Fe������ˮ������Ӧ�����ɵ�H2������ĿΪ0.3NA
B. �����£�1 L pH=13��NaOH��Һ�У���ˮ�����OH��������ĿΪ0.1NA
C. ����ȼ�ϵ����������22.4 L����״��������ʱ����·��ͨ���ĵ�����ĿΪ2NA
D. 5NH4NO3![]() 2HNO3+4N2��+9H2O��Ӧ�У�����28 g N2ʱ��ת�Ƶĵ�����ĿΪ3.75NA
2HNO3+4N2��+9H2O��Ӧ�У�����28 g N2ʱ��ת�Ƶĵ�����ĿΪ3.75NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�Ȼ�ѧ����ʽ:2SO2(g)+O2(g) ![]() 2SO3(g)����H=-Q kJ��mol-1(Q>0)������˵����ȷ����(����)
2SO3(g)����H=-Q kJ��mol-1(Q>0)������˵����ȷ����(����)
A. ��ͬ������,2 mol SO2(g)��1 mol O2(g)�����е�����С��2 mol SO3(g)�����е�����
B. ��2 mol SO2(g)��1 mol O2(g)����һ�ܱ������г�ַ�Ӧ��,�ų�������ΪQ kJ
C. ��ʹ�ô���,�÷�Ӧ��|��H|��С
D. �罫һ����SO2(g)��O2(g)����ij�ܱ������г�ַ�Ӧ�����Q kJ,��˹�������2 molSO2(g)������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪![]() ��Ϊͬ���칹�壬����˵������ȷ����
��Ϊͬ���칹�壬����˵������ȷ����
A. z�Ķ��ȴ���������
B. x��y��һ�ȴ����ֻ������
C. x��y ��ʹ������Ȼ�̼��Һ�����ӳɷ�Ӧ����ɫ
D. x��y��z��ֻ��x������ԭ�ӿ��ܴ���ͬһƽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ��������250 mL 0.1 mol��L��1Na2CO3��Һʱ������Ҫ�õ��������ǣ� ��
A.����ƿB.�ձ�C.������D.�ƾ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ᱵ��BaTiO3���ڹ�ҵ������Ҫ��;����Ҫ�������������մɡ�PTC�������衢�������ȶ��ֵ���Ԫ�����������������ᱵ��һ�ֹ�������ͼ��
![]()
��֪��25��ʱ��BaCO3���ܶȻ�Ksp=2.58��10-9��
��1��BaTiO3��TiԪ�صĻ��ϼ�Ϊ��________��
��2�����������ʱ��Ϊʹ������ʼӿ죬�ɲ�ȡ��һ�ִ�ʩ�ǣ�____________________��������Ӧ�����ӷ���ʽΪ��____________________________________��
��3��������ͨ�����˵õ����������ѱ����壬���˲�����ʹ�õIJ��������У�______________��
��4��TiO2���кܺõ�ɢ���ԣ���һ������Ҫ��;�Ľ����������ҵ�Ͽ���TiCl4ˮ�����Ʊ����Ʊ�ʱ����������ˮ��ͬʱ���ȣ���Ŀ���ǣ�___________________________��
��5��ij��ȤС��ȡ19.70gBaCO3ģ���������������Ʊ�BaTiO3���ò�Ʒ13.98g��BaTiO3�IJ���Ϊ��___________��
��6���������������������ʵ����BaCO3�ܽ�ƽ����ƶ���������Һ��c(Ba2+)=0.1mol��L-1����c(CO32-)�ڽ���Һ�е����Ũ��Ϊ��_________mol��L-1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ŀǰ������60%��þ�ǴӺ�ˮ����ȡ�ģ���ͼ��ij�����Ӻ�ˮ����ȡþ����Ҫ���衣ѧ�����������չ�������ۡ�
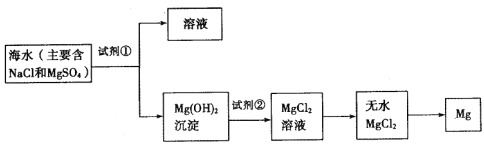
ѧ�����������������������⣺
(һ)�ں�ˮ��þ�Ĺ��������ʵ�ֶ�þ���ӵĸ�����������ѧ������Լ��Ĺ۵㡣
ѧ���Ĺ۵㣺ֱ������ˮ�м����������
ѧ���ҵĹ۵㣺���¼���������ˮ���ټ����������
ѧ�����Ĺ۵㣺����ɹ�κ�Ŀ�±ˮ���ټ����������
ͨ�������Ƚ�����Ϊѧ��_______�Ĺ۵���ȷ(��ѧ�����)���������ɣ�______________________��
(��)�ں�ˮ��þ�Ĺ��������ʵ�ֶ�þ���ӵķ��룿
(1)Ϊ��ʹþ���ӳ�����������������õ��صı���(��Ҫ�ɷ�Ϊ̼���)��Դ������������Լ�����___________(�ѧʽ)��
(2)�����Լ������ܹ�����õ�Mg(OH)2�����ķ�����_________(������ĸ)
A������ B������ C����ȡ D����Һ
(3)����������Լ�����______________________(�ѧʽ)��
(4)д������ˮMgCl2��ȡ����þ�Ļ�ѧ����ʽ________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ˮ������Ҫ�Ľ������ϡ�ˮ�����ϵ���Ҫ�ɷ�ΪCaO��SiO2��������һ��������������þ�Ƚ����������ʵ���Ҳⶨˮ����Ʒ�иƺ����Ĺ�����ͼ��ʾ��
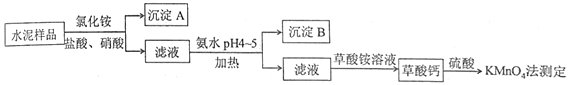
�ش��������⣺
��1���ڷֽ�ˮ����Ʒ�����У�������Ϊ�ܼ����Ȼ��Ϊ���ܼ���������뼸�����ᡣ���������Ŀ����__________������ʹ��___________�������ᡣ
��2������A����Ҫ�ɷ���_________���䲻����ǿ�ᵫ����һ�����ᷴӦ���÷�Ӧ�Ļ�ѧ����ʽΪ____________________________________��
��3���Ӱ�ˮ�����м��ȵ�Ŀ����___________������B����Ҫ�ɷ�Ϊ_____________��____________���ѧʽ����
��4������Ƴ�����ϡH2SO4��������KMnO4����Һ�ζ���ͨ���ⶨ��������ɼ�ӻ�֪�Ƶĺ������ζ���ӦΪ�� ![]() +H++H2C2O4��Mn2++CO2+H2O��ʵ���г�ȡ0.400 gˮ����Ʒ���ζ�ʱ������0.0500 mol��L-1��KMnO4��Һ36.00 mL�����ˮ����Ʒ�иƵ���������Ϊ______________��
+H++H2C2O4��Mn2++CO2+H2O��ʵ���г�ȡ0.400 gˮ����Ʒ���ζ�ʱ������0.0500 mol��L-1��KMnO4��Һ36.00 mL�����ˮ����Ʒ�иƵ���������Ϊ______________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com