
在一定温度下,将气体X和气体Y各0. 16 mol充入2 L恒容密闭容器中,发生反应
X(g)+Y(g)=2Z(g) ,一段时间后达到平衡。反应过程中测定的数据如下表:
| t/min | 2 | 4 | 7 | 9 |
| n(X)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是( )
A、反应前2 min的平均速率ν(Z)=0.04mol/(L·min)
B.保持其他条件不变,若升高温度,平衡时c(X)= 0.06 mol·L-1,则该反应的H>0
C.相同温度下,起始时向容器中充入1mol X、0.2mol Y 和0.2mol Z,反应达到平衡前v(正)>v(逆)
D、其他条件不变,从反应体系中移走一部分 Z,正反应速率增大,逆反应速率减小,平衡正向移动
科目:高中化学 来源: 题型:
原子结构模型的演变图如图:

其中,(1)为道尔顿实心球式原子模型;(2)为卢瑟福行星运转式原子模型;(3)为汤姆生葡萄干面包式原子模型;(4)为近代量子力学原子模型;(5)为玻尔轨道式原子模型.下列符合历史演变顺序的一组排列是()
A. (1)(3)(2)(5)(4) B. (1)(2)(3)(4)(5) C. (1)(5)(3)(2)(4) D. (1)(3)(5)(4)(2)
查看答案和解析>>
科目:高中化学 来源: 题型:
某元素的一种核素X的质量数为A,含N个中子,它与1H原子组成HmX分子,在ag HmX中所含质子的物质的量是()
A.  (A﹣N+m)mol B.
(A﹣N+m)mol B.  (A﹣N)mol C.
(A﹣N)mol C.  (A﹣N)mol D.
(A﹣N)mol D. 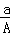 (A﹣N+m)mol
(A﹣N+m)mol
查看答案和解析>>
科目:高中化学 来源: 题型:
一般情况下,较强的氧化剂如:MnO2、KMnO4、KClO3、Ca(ClO)2等氧化浓盐酸时,有如下反应规律:氧化剂+浓盐酸→金属氯化物+水+氯气.实验室通常用该原理制取少量Cl2.现将214.5gCa(ClO)2放入500 mL 12.0 mol/L的浓盐酸中,生成的Cl2在标准状况下的体积为39.2 L.试计算:
(1)该反应消耗的氧化剂的质量是 g
(2)若反应前后溶液的体积保持不变,则反应后溶液中HCl的物质的量浓度为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,某化学学习小组借助下列装置(夹持装置已略)及相关试剂粗略测量空气中O2的体积百分数。
(1) 实验前用碱液清洗铁钉,再用0.100mol/L的 H2SO4溶液浸泡至有气泡产生。用H2SO4溶液浸泡的目的是______。
(2) 为尽量减小误差,下列操作的正确顺序是______(填序号)。
①装入铁钉
②插入注射器向铁钉表面滴入适量 NaCl溶液并打开止水夹
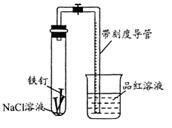 ③将导管口浸入品红溶液
③将导管口浸入品红溶液
④塞上单孔活塞
⑤检查装置气密性
(3) 检查装置气密性的方法:_______________________________。
(4)实验中试管内发生的反应为:____________________________。
用该实验方案测量空气中O2的体积百分数时应测量的数据是:①导管与试管内部空间总体积,
②__________________________________________。
(5) 实验时发现上述测量过程因反应较慢耗时较长,对其影响因素作如下分析:
假设一:电解质溶液的PH 假设二: NaCl溶液的浓度 假设三:铁钉的表面积
(6)借助上述实验装置,通过调节溶液的pH验证假设一,获得了如下实验数据:
①当pH=2时,没有观察到稳定液柱形成的原因是______
②根据实验数据分析,为缩短实验测定时间,pH的最佳范围是______
③按上述实验装置,设计实验证明假设二。
第一步:____________;
第二步: ______,分别用注射器将NaCl溶液滴入铁钉表面;
第三步:记录形成稳定液柱所用时间和液柱的高度,比较分析数据得出结论。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com