
. |
| M |
| m |
| n |


 ����С��ʿ���������ϵ�д�
����С��ʿ���������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| �¶�/�� | 250 | 310 | 350 |
| K | 2.041 | 0.250 | 0.012 |
| Ũ��mol/L ʱ��/min |
c��CO�� | c��H2�� | c��CH3OH�� |
| 0 | 0.8 | 1.6 | 0 |
| 2 | 0.6 | 1.2 | 0.2 |
| 4 | 0.3 | 0.6 | 0.5 |
| 6 | 0.3 | 0.6 | 0.5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ���ӱ�ʡ��ˮ��ѧ2012��������Ĵε��п��Ի�ѧ���� ���ͣ�058
ú��������úΪԭ�ϣ�������ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ���̣�
(1)��ú��������Ӧ���з������¼��ַ�Ӧ��
C(s)ʮH2O(g)��CO(g)��H2(g)����H����131 kJ/mol
C(s)��O2(g)��CO2(g)����H����394 kJ/mol
CO(g)��![]() O2(g)��CO2(g)����H����283 kJ/mol
O2(g)��CO2(g)����H����283 kJ/mol
��CO(g)��H2O(g)![]() H2(g)��CO2(g)����H��________
H2(g)��CO2(g)����H��________
(2)��֪830��ʱ����һ���ݻ��̶����ܱ������У�������Ӧ
CO(g)��H2O(g)![]() H2(g)��CO2(g)�������жϸ÷�Ӧ�ﵽ��ѧƽ��״̬����________(����ĸ)��
H2(g)��CO2(g)�������жϸ÷�Ӧ�ﵽ��ѧƽ��״̬����________(����ĸ)��
a�������е�ѹǿ����
b��1 mol��H��H�����ѵ�ͬʱ����2 mol��H��O��
c��v��(CO)��v��(H2O)
d��c(CO)��c(H2)
��֪���¶��¸÷�Ӧ��ƽ�ⳣ��K��1�������ʵ�����CO��H2O��Ӧ�ﵽƽ��ʱ��CO��ת����Ϊ________��
(3)����ͬ����CO(g)��H2O(g)�ֱ�ͨ�뵽���Ϊ2 L�ĺ����ܱ������У����з�ӦCO(g)��H2O(g)![]() H2(g)��CO2(g)���õ������������ݣ�
H2(g)��CO2(g)���õ������������ݣ�
��ʵ��1����v(CO2)��ʾ�ķ�Ӧ����Ϊ________��
�ڸ÷�Ӧ���淴ӦΪ________(������š���)�ȷ�Ӧ
����ʵ��3Ҫ�ﵽ��ʵ��2��ͬ��ƽ��״̬(�������ʵ����������ֱ����)����t��3 min����a��bӦ����Ĺ�ϵ��________(�ú�a��b����ѧʽ��ʾ)��
(4)Ŀǰ��ҵ����һ�ַ�������CO2�������״���һ�������·�����Ӧ��3H2(g)��CO2(g)![]() CH3OH(g)��H2O(g)����ͼ��ʾ
CH3OH(g)��H2O(g)����ͼ��ʾ
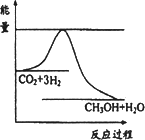
�÷�Ӧ���й���������(��λΪkJ��mol)�ı仯��
�������Ϊ1 L�ĺ����ܱ������У�����1 mol��CO2��3 mol��H2�����д�ʩ����ʹc(CH3OH)�������________(����ĸ)
a�������¶�
b������He(g)��ʹ��ϵѹǿ����
c����H2O(g)����ϵ�з������
d���ٳ���1 mol��CO2��3 mol��H2
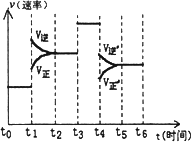
�ڵ���Ӧ�ﵽƽ��ʱ���ϸı�����(�����ı��������ʵ�����״̬��ֻ�ı�һ������)��Ӧ������ʱ��ı仯����ͼ�����б�ʾƽ��������CH3OH������ߵ�һ��ʱ����________����t0��t1ƽ�ⳣ��ΪK1��t2��t3ƽ�ⳣ��ΪK2����K1________K2(����ڡ��������ڡ���С�ڡ�)��
(5)ú���������л���������CH4����֪CH4��CaSO4��Ӧ����CaS��CO2��H2O���÷�Ӧ���������뻹ԭ�������ʵ���֮��Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012��ӱ�ʡ��ˮ��ѧ������ѧ���ĵ����Ի�ѧ�Ծ� ���ͣ������
ú��������úΪԭ�ϣ�������ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ���̡�(1) ��ú��������Ӧ���з������¼��ַ�Ӧ��
C��s��ʮH2O��g��=CO��g��+H2��g�� ��H= +131kJ/mol
C��s��+O2��g��=CO2��g�� ��H= ��394kJ/mol
CO��g��+ O2��g��=CO2��g�� ��H= ��283kJ/mol
O2��g��=CO2��g�� ��H= ��283kJ/mol
��CO��g��+H2O��g�� H2��g��+CO2��g����H=
H2��g��+CO2��g����H=
��2����֪830��ʱ����һ���ݻ��̶����ܱ������У�������Ӧ
CO��g��+H2O��g�� H2��g��+CO2��g���������жϸ÷�Ӧ�ﵽ��ѧƽ��״̬���� (����ĸ)��
H2��g��+CO2��g���������жϸ÷�Ӧ�ﵽ��ѧƽ��״̬���� (����ĸ)��
a�������е�ѹǿ���� b��1 mol H-H�����ѵ�ͬʱ����2 mol H-O��
c��  (CO)=
(CO)=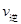 (H2O) d��c(CO)=c(H2)
(H2O) d��c(CO)=c(H2)
��֪���¶��¸÷�Ӧ��ƽ�ⳣ��K=1�������ʵ�����CO��H2O��Ӧ�ﵽƽ��ʱ��CO��ת����Ϊ .
(3) ����ͬ����CO(g)��H2O(g)�ֱ�ͨ�뵽���Ϊ2 L�ĺ����ܱ������У����з�Ӧ
CO��g��+H2O��g�� H2��g��+CO2��g�����õ������������ݣ�
H2��g��+CO2��g�����õ������������ݣ�
��ʵ��l���� (CO2)��ʾ�ķ�Ӧ����Ϊ ��
(CO2)��ʾ�ķ�Ӧ����Ϊ ��
�ڸ÷�Ӧ���淴ӦΪ (������š���)�ȷ�Ӧ
����ʵ��3Ҫ�ﵽ��ʵ��2��ͬ��ƽ��״̬(�������ʵ����������ֱ����)����t<3min����a��bӦ����Ĺ�ϵ�� (�ú�a��b����ѧʽ��ʾ)��
(4)Ŀǰ��ҵ����һ�ַ�������CO2�������״���һ�������·�����Ӧ��
3H2��g��+CO2��g�� CH3OH��g��+H2O��g������ͼ��ʾ
CH3OH��g��+H2O��g������ͼ��ʾ
�÷�Ӧ���й���������(��λΪkJ��mol)�ı仯��
�������Ϊ1 L�ĺ����ܱ������У�����l molCO2��3molH2�����д�ʩ����ʹc(CH3OH)������� (����ĸ)
a�������¶� b������He(g)��ʹ��ϵѹǿ����
c����H2O(g)����ϵ�з������ d���ٳ���l mol CO2��3 molH2
�ڵ���Ӧ�ﵽƽ��ʱ���ϸı�����(�����ı�
��������ʵ�����״̬��ֻ�ı�һ������)��Ӧ������ʱ��ı仯����ͼ�����б�ʾƽ��������CH3OH������ߵ�һ��ʱ���� ����t0��t1ƽ�ⳣ��ΪK1,t2��t3ƽ�ⳣ��ΪK2����K1 K2(����ڡ��������ڡ���С�ڡ�)��
��5��ú���������л���������CH4����֪CH4��CaSO4��Ӧ����CaS��CO2��H2O���÷�Ӧ���������뻹ԭ�������ʵ���֮��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ���㽭ʡ������ʮ��У�����ڶ����������ۻ�ѧ�Ծ��������棩 ���ͣ������
2013��9�£��й��������е������������ص������������������ӱ������ϵȵصĿ�����Ⱦ��Ϊ6��������Ⱦ�������ض���Ⱦ������β����ȼú����������ȡů�ŷŵ�CO2�ȶ��������γɵ�ԭ��
��1������β����������Ҫԭ��Ϊ;2NO(g)��2CO(g)  N2��g)��2CO2��g)�� ��H��0����һ���¶��£���һ����̶����ܱ������г���һ������NO��CO��t1ʱ�̴ﵽƽ��״̬��
N2��g)��2CO2��g)�� ��H��0����һ���¶��£���һ����̶����ܱ������г���һ������NO��CO��t1ʱ�̴ﵽƽ��״̬��
�����жϸ÷�Ӧ�ﵽƽ��״̬�ı�־�ǣߣߣߣߡ�
A.�ڵ�λʱ��������1mol CO2��ͬʱ������lmol CO
B�����������ܶȲ��ٸı�
C.��������ƽ����Է����������ٸı�
D.��������ѹǿ���ٱ仯
����t2ʱ�̣����������ݻ�Ѹ������ԭ����2�����������������������£�t3ʱ�̴ﵽ�µ�ƽ��״̬��֮���ٸı�������������ͼ�в��仭����t2��t4ʱ������Ӧ������ʱ��ı仯���ߣ�
?? 
����Ҫͬʱ��߸÷�Ӧ�����ʺ�NO��ת���ʣ���ȡ�Ĵ�ʩ��_____��____����д��2����
(2���ı�ú�����÷�ʽ�ɼ��ٻ�����Ⱦ��ͨ���ɽ�ˮ����ͨ�����ȵ�̼�õ�ˮú�����䷴Ӧԭ��ΪC(s)��H2O(g) CO(g)��H2(g) ��H��+131.3kJ/mol��
CO(g)��H2(g) ��H��+131.3kJ/mol��
�ٸ÷�Ӧ��___�����Է����У�����¡����¡�����
��ú���������в������к�����H2S����������Na2C03��Һ���գ��÷�Ӧ�����ӷ���ʽΪ____������֪��H2S�� Ka1��9.1��10-8��Ka2��1.1��10-12��H2CO3��Ka1��4.30��10-7��Ka2��5.61��10-11��
(3����֪��Ӧ��CO(g����H2O��g�� CO2��g����H2��g�����ֽ���ͬ����CO��g����H2O��g���ֱ�ͨ�˵����Ϊ2L�ĺ����ܱ������н��з�Ӧ���õ������������ݣ�
CO2��g����H2��g�����ֽ���ͬ����CO��g����H2O��g���ֱ�ͨ�˵����Ϊ2L�ĺ����ܱ������н��з�Ӧ���õ������������ݣ�
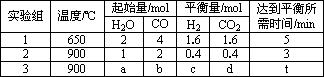
ʵ�� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | ��ƽ������ʱ��/min | ||
CO | H2O | H2 | CO | |||
1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
3 | 900 | a | b | c | d | t |
��ʵ��1������ƽ�ⳣ��K��______������С������λ����
��ʵ��3�У���ƽ��ʱ��CO��ת���ʴ���ˮ��������a��b��������Ĺ�ϵ��______��
�۸÷�Ӧ�ġ�H ______0(�����������������9000Cʱ������һ��ʵ�飬�ڴ������м���l0mol CO,5mo1 H2O,2mo1 CO2,5mol H2�����ʱ����______�������������������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
(14��)ú��������úΪԭ�ϣ�������ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ���̡�
(1) ��ˮ����ͨ�����ȵ�̼���ɲ���ˮú������ӦΪ��
![]()
һ���¶��£���һ���ݻ��̶����ܱ������У�����������Ӧ���������жϸ÷�Ӧ�ﵽ��ѧƽ��״̬���� (����ĸ)��
a�������е�ѹǿ���� b��1 mol H-H�����ѵ�ͬʱ����2 mol H-O��
c�� ![]() =(CO)=
=(CO)=![]() (H2O) d��c(CO)=c(H2)
(H2O) d��c(CO)=c(H2)
(2) ����ͬ����CO(g)��H2O(g)�ֱ�ͨ�뵽���Ϊ2 L�ĺ����ܱ������У����з�Ӧ
![]() ���õ������������ݣ�
���õ������������ݣ�
ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
|
|
|
| |||
1 | 650 | 2 | 4 | 1.6 | 1.6 | 5 |
2 | 900 | 1 | 2 | 0.4 | 0.4 | 3 |
3 | 9.. | a | b | c | d | t |
��ʵ��l����![]() (CO2)��ʾ�ķ�Ӧ����Ϊ ��
(CO2)��ʾ�ķ�Ӧ����Ϊ ��
�ڸ÷�Ӧ���淴ӦΪ (������š���)�ȷ�Ӧ
����ʵ��3Ҫ�ﵽ��ʵ��2��ͬ��ƽ��״̬(�������ʵ����������ֱ����)����t<3min����a��bӦ����Ĺ�ϵ�� (�ú�a��b����ѧʽ��ʾ)��
(3)Ŀǰ��ҵ����һ�ַ�������CO2�������״���һ�������·�����Ӧ��
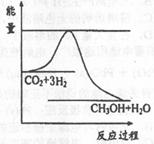
![]() ��ͼ��ʾ
��ͼ��ʾ
�÷�Ӧ���й���������(��λΪlkJ?mol��)�ı仯��
�������Ϊ1 L�ĺ����ܱ������У�����l molCO2��3molH2�����д�ʩ����ʹc(CH3OH)������� (����ĸ)
a�������¶�
b������He(g)��ʹ��ϵѹǿ����
c����H2O(g)����ϵ�з������
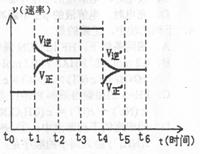 d���ٳ���l mol CO2��3 molH2
d���ٳ���l mol CO2��3 molH2
�ڵ���Ӧ�ﵽƽ��ʱ���ϸı�����(�����ı��������ʵ�����״̬)��Ӧ������ʱ��ı仯����ͼ�����б�ʾƽ��������CH3OH������ߵ�һ��ʱ���� ����t0��t1ƽ�ⳣ��Ϊ��K1,t2��t3ƽ�ⳣ��ΪK2����K1 K2(����ڡ��������ڡ���С�ڡ�)��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com