
下列离子方程式,书写正确的是( )
A.氯气溶于水:Cl2+H2O=2H++Cl-+ClO-
B.硫酸铝溶液中加入足量氨水:Al3++4OH-=[Al(OH)4]-
C.FeSO4溶液与稀硝酸反应:3Fe2++NO3—+4H+=3Fe3++NO↑+2H2O
D.碳酸氢铵和足量氢氧化钠溶液反应:NH4++OH-=NH3·H2O
科目:高中化学 来源:2013-2014学年高考化学二轮复习提分训练 专题5化学反应与能量练习卷(解析版) 题型:选择题
在同温同压下,下列各组热化学方程式中ΔH1>ΔH2的是( )。
A.2H2(g)+O2(g)=2H2O(l) ΔH1 2H2(g)+O2(g)=2H2O(g) ΔH2
B.S(g)+O2(g)=2SO2(g) ΔH1 S(s)+O2(g)=2SO2(g) ΔH2
C.C(s)+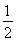 O2(g)=CO(g) ΔH1 C(s)+O2(g)=CO2(g) ΔH2
O2(g)=CO(g) ΔH1 C(s)+O2(g)=CO2(g) ΔH2
D.H2(g)+Cl2(g)=2HCl(g) ΔH1  H2(g)+
H2(g)+ Cl2(g)=HCl(g) ΔH2
Cl2(g)=HCl(g) ΔH2
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习提分训练 专题10金属元素及其化合物练习卷(解析版) 题型:选择题
工业上用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下:

下列叙述正确的是( )。
A.试剂X可以是氢氧化钠溶液,也可以是盐酸
B.反应①、过滤后所得沉淀为氢氧化铁
C.图中所示转化反应都不是氧化还原反应
D.反应②的化学方程式为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 综合实验设计与评价练习卷(解析版) 题型:选择题
下列制取气体的方案,可以直接采用如图所示装置进行的有( )

①用H2O2和MnO2制取O2
②用CaCO3和稀盐酸制取CO2
③用KClO3和MnO2制取O2
④用Zn和稀H2SO4制取H2
⑤用Cu和浓HNO3制取NO2
A.①④ B.①②④ C.①②⑤ D.①②④⑤
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 离子反应、氧化还原反应练习卷(解析版) 题型:选择题
下列反应中,氧化剂与还原剂的物质的量之比为1:2的是
①O3+2KI+H2O=2KOH+I2+O2 ②SiO2+2C Si+2CO↑
Si+2CO↑
③SiO2+3C SiC+2CO↑ ④4HCl(浓)+MnO2
SiC+2CO↑ ④4HCl(浓)+MnO2 MnCl2+Cl2↑+2H2O( )
MnCl2+Cl2↑+2H2O( )
A.仅有② B.②④ C.②③④ D.①②③④
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 电解质溶液练习卷(解析版) 题型:填空题
某铵态氮肥由W、X、Y、Z 4种短周期元素组成,其中W的原子半径最小。
Ⅰ.若Y、Z同主族,ZY2是形成酸雨的主要物质之一。
(1)将X、Y、Z的元素符号填在如图所示元素周期表(局部)中的相应位置上。

(2)X的最高价氧化物对应水化物的稀溶液与铜反应的化学方程式为 。
(3)一定条件下,1 mol XW3气体与O2完全反应生成X元素的单质和液态水,放出382.8 kJ热量。该反应的热化学方程式为 __。
Ⅱ.若Z是形成化合物种类最多的元素。
(4)该氮肥的名称是 __(填一种)。
(5)HR是含Z元素的一元酸。室温时,用0.250 mol·L-1NaOH溶液滴定25.0 mL HR溶液时,溶液的pH变化情况如图所示。

其中,a点表示两种物质恰好完全反应。
①图中x (填“>”“<”或“=”)7。
②室温时,HR的电离常数Ka= (填数值)。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 电解质溶液练习卷(解析版) 题型:选择题
常温下,将一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如表:
实验编号 | c(HA)/mol·L-1 | c(NaOH)/mol·L-1 | 混合溶液的pH |
甲 | 0.1 | 0.1 | pH=a |
乙 | 0.2 | 0.2 | pH=9 |
丙 | c1 | 0.2 | pH=7 |
丁 | 0.2 | 0.1 | pH<7 |
下列判断正确的是( )
A.a>9
B.在乙组混合液中由水电离出的c(OH-)=10-5mol·L-1
C.c1<0.2
D.丁组混合液:c(Na+)>c(A-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 电化学原理及其应用练习卷(解析版) 题型:选择题
电解原理在化学工业中有着广泛的应用。图甲表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。则下列说法不正确的是( )

A.若此装置用于电解精炼铜,则X为纯铜、Y为粗铜,电解的溶液a可以是硫酸铜或氯化铜溶液
B.按图甲装置用惰性电极电解AgNO3溶液,若图乙横坐标x表示流入电极的电子的物质的量,则E可表示反应生成硝酸的物质的量,F表示电解生成气体的物质的量
C.按图甲装置用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,加入0.5 mol的碳酸铜刚好恢复到通电前的浓度和pH,则电解过程中转移的电子为2.0 mol
D.若X、Y为铂电极,a溶液为500 mL KCl和KNO3的混合液,经过一段时间后,两极均得到标准状况下11.2 L气体,则原混合液中KCl的物质的量浓度至少为2.0 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 物质的量及其应用练习卷(解析版) 题型:选择题
设nA为阿伏加德罗常数的数值,下列说法正确的是( )
A.常温常压下,8 g O2含有4nA个电子
B.1 L 0.1 mol·L-1的氨水中有nA个NH4+
C.标准状况下,22.4 L盐酸含有nA个HCl分子
D.1 mol Na被完全氧化生成Na2O2,失去2nA个电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com