
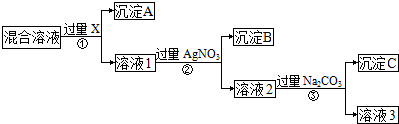
·ÖĪö ³żČ„ČÜŅŗÖŠµÄNaClŗĶNa2SO4£¬“Ó¶ųµĆµ½“æ¾»µÄNaNO3ČÜŅŗ£¬ÓÉŹµŃéĮ÷³ĢæÉÖŖ£¬ČēĻČ¼ÓČėAgNO3£¬Ōņ»įĶ¬Ź±Éś³ÉAg2SO4ŗĶAgCl³Įµķ£¬ŌņÓ¦ĻČ¼ÓČė¹żĮæµÄXĪŖBaCl2[»ņBa£ØNO3£©2]£¬Éś³É³ĮµķAĪŖBaSO4³Įµķ£¬Č»ŗóŌŚČÜŅŗ1ÖŠ¼ÓČė¹żĮæµÄAgNO3£¬Ź¹Cl-Č«²æ×Ŗ»ÆĪŖAgCl³Įµķ£¬¼“³ĮµķBĪŖAgCl£¬ŌŁĻņĖłµĆČÜŅŗ2ÖŠ¼ÓČė¹żĮæµÄNa2CO3£¬Ź¹ČÜŅŗÖŠµÄAg+”¢Ba2+ĶźČ«³Įµķ£¬³ĮµķCĪŖĢ¼Ėį±µ”¢Ģ¼ĖįŅų£¬×īŗóĖłµĆČÜŅŗ3ĪŖNaNO3ŗĶNa2CO3µÄ»ģŗĻĪļ£¬¼ÓČėĻ”HNO3£¬×īŗó½ųŠŠÕō·¢²Ł×÷æÉµĆ¹ĢĢåNaNO3£¬ŅŌ“ĖĄ“½ā“š£®
½ā“š ½ā£ŗ³żČ„ČÜŅŗÖŠµÄNaClŗĶNa2SO4£¬“Ó¶ųµĆµ½“æ¾»µÄNaNO3ČÜŅŗ£¬ÓÉŹµŃéĮ÷³ĢæÉÖŖ£¬ČēĻČ¼ÓČėAgNO3£¬Ōņ»įĶ¬Ź±Éś³ÉAg2SO4ŗĶAgCl³Įµķ£¬ŌņÓ¦ĻČ¼ÓČė¹żĮæµÄXĪŖBaCl2[»ņBa£ØNO3£©2]£¬Éś³É³ĮµķAĪŖBaSO4³Įµķ£¬Č»ŗóŌŚČÜŅŗ1ÖŠ¼ÓČė¹żĮæµÄAgNO3£¬Ź¹Cl-Č«²æ×Ŗ»ÆĪŖAgCl³Įµķ£¬¼“³ĮµķBĪŖAgCl£¬ŌŁĻņĖłµĆČÜŅŗ2ÖŠ¼ÓČė¹żĮæµÄNa2CO3£¬Ź¹ČÜŅŗÖŠµÄAg+”¢Ba2+ĶźČ«³Įµķ£¬³ĮµķCĪŖĢ¼Ėį±µ”¢Ģ¼ĖįŅų£¬×īŗóĖłµĆČÜŅŗ3ĪŖNaNO3ŗĶNa2CO3µÄ»ģŗĻĪļ£¬¼ÓČėĻ”HNO3£¬×īŗó½ųŠŠÕō·¢²Ł×÷æÉµĆ¹ĢĢåNaNO3£¬
£Ø1£©øł¾ŻÉĻĆęµÄ·ÖĪöæÉÖŖ£¬ŹµŃé×īÖÕŅŖµĆµ½NaNO3£¬ŹŌ¼ĮX×īŗĆŹĒBa£ØNO3£©2£¬¼ģŃéBa£ØNO3£©2ŹĒ·ń¼ÓČė¹żĮæµÄ·½·ØŹĒČÜŅŗ¾²ÖĆ·Ö²ć£¬¼ĢŠųµĪ¼ÓBa£ØNO3£©2£¬ČōĪŽ³ĮµķÉś³É£¬ŌņĖµĆ÷Ba£ØNO3£©2ŅŃ¾¹żĮ棬·ńŌņƻӊ¹żĮ棬
¹Ź“š°øĪŖ£ŗBa£ØNO3£©2£»ČÜŅŗ¾²ÖĆ·Ö²ć£¬¼ĢŠųµĪ¼ÓBa£ØNO3£©2£¬ČōĪŽ³ĮµķÉś³É£¬ŌņĖµĆ÷Ba£ØNO3£©2ŅŃ¾¹żĮ棬·ńŌņƻӊ¹żĮ棻
£Ø2£©²½Öč¢ŚµÄĄė×Ó·“Ó¦·½³ĢŹ½ĪŖAg++Cl-ØTAgCl”ż£¬¹Ź“š°øĪŖ£ŗAg++Cl-ØTAgCl”ż£»
£Ø3£©øł¾ŻÉĻĆęµÄ·ÖĪöæÉÖŖ£¬°““ĖŹµŃé·½°øµĆµ½µÄČÜŅŗ3ÖŠæĻ¶Øŗ¬ÓŠNa2CO3ŌÓÖŹ£¬ĪŖĮĖ³żÕāøöŌÓÖŹ£¬æÉŅŌĻņČÜŅŗ3ÖŠ¼ÓČė¹żĮæµÄHNO3£¬Ö®ŗóČōŅŖ»ńµĆ“æ¹ĢĢåNaNO3£¬»¹Šč½ųŠŠµÄŹµŃé²Ł×÷ŹĒÕō·¢£¬
¹Ź“š°øĪŖ£ŗNa2CO3£»HNO3£»Õō·¢£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹµÄ·ÖĄėĢį“æ²Ł×÷£¬ĢāÄæÄѶČÖŠµČ£¬±¾Ģā×¢ŅāCl-”¢SO42-µÄŠŌÖŹ£¬°ŃĪÕ³żŌÓŌŌņ£¬Ģį“æŹ±²»ÄÜŅżČėŠĀµÄŌÓÖŹ£¬×¢Ņā°ŃĪÕŹµŃéµÄĻČŗóĖ³Šņ£®


 ½Ģ²ÄČ«½ā×Ö“Ź¾äĘŖĻµĮŠ“š°ø
½Ģ²ÄČ«½ā×Ö“Ź¾äĘŖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| X | Y | |
| Z | W |
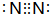 £»YŗĶĒāŌŖĖŲŠĪ³ÉµÄ10µē×ÓĪ¢Į£ÖŠ³£¼ūµÄ+1¼ŪŃōĄė×ÓĪŖH3O+£ØĢī»ÆѧŹ½£¬ĻĀĶ¬£©£»ZŗĶĒāŌŖĖŲŠĪ³ÉµÄ18µē×ÓĪ¢Į£ÖŠ³£¼ūµÄ-1¼ŪŅõĄė×ÓĪŖHS-£»
£»YŗĶĒāŌŖĖŲŠĪ³ÉµÄ10µē×ÓĪ¢Į£ÖŠ³£¼ūµÄ+1¼ŪŃōĄė×ÓĪŖH3O+£ØĢī»ÆѧŹ½£¬ĻĀĶ¬£©£»ZŗĶĒāŌŖĖŲŠĪ³ÉµÄ18µē×ÓĪ¢Į£ÖŠ³£¼ūµÄ-1¼ŪŅõĄė×ÓĪŖHS-£»²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £¬AŌŚŅ»¶ØĢõ¼žĻĀÄÜÓėĖ®·“Ó¦£¬æÉÓĆÓŚŅūÓĆĖ®µÄĻū¶¾£¬ŹŌŠ“³ö“Ė·“Ó¦µÄ»Æѧ·“Ó¦·½³ĢŹ½NCl3+3H2O=NH3+3HClO£®
£¬AŌŚŅ»¶ØĢõ¼žĻĀÄÜÓėĖ®·“Ó¦£¬æÉÓĆÓŚŅūÓĆĖ®µÄĻū¶¾£¬ŹŌŠ“³ö“Ė·“Ó¦µÄ»Æѧ·“Ó¦·½³ĢŹ½NCl3+3H2O=NH3+3HClO£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŚ±„ŗĶĀČĖ®ÖŠ£ŗCl-”¢NO3-”¢Na+”¢SO32- | |
| B£® | 0.1mol/L NaAlO2ČÜŅŗÖŠ£ŗK+”¢CO32-”¢SO42-”¢Cl- | |
| C£® | ŌŚĒæ¼īŠŌČÜŅŗÖŠ£ŗNa+”¢NH4+”¢SO32-”¢Cl- | |
| D£® | 1.0mol•L-1µÄŃĪĖįČÜŅŗÖŠ£ŗK+”¢Fe2+”¢ClO-”¢SO42- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ČÜŅŗµÄpH | ¼ÓČėŃĪĖįµÄ×ÜĢå»ż |
| 12 | V£ØHCl£©=0 |
| 8 | V£ØHCl£©=20.00mL |
| 5 | V£ØHCl£©=40.00mL |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ${\;}_{77}^{192}$IrŗĶ${\;}_{77}^{193}$IrŹĒĮ½ÖÖŗĖĖŲ | |
| B£® | ${\;}_{77}^{192}$IrŗĶ${\;}_{77}^{193}$IrŹĒĮ½ÖÖŌŖĖŲ | |
| C£® | IrŹĒÖ÷×åŌŖĖŲ | |
| D£® | ÓÉ${\;}_{77}^{193}$Ir¾¹żÖŠ×Ó·ųÉäŗó»ńµĆ${\;}_{77}^{192}$IrŹĒ»Æѧ±ä»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | NH4+£¬NO3-£¬CO32-£¬Na+ | B£® | Na+£¬Ba2+£¬Mg2+£¬HCO3- | ||
| C£® | NO3-£¬Ca2+£¬K+£¬H+ | D£® | NO3-£¬K+£¬AlO2-£¬OH- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | BaCl2”śNa2CO3 | B£® | Na2CO3”śHCl | C£® | Na2CO3”śCa£ØOH£©2 | D£® | Ė®”śBaCl2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±½¼×“¼£ŗC6H5CH2OH | B£® | 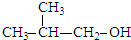 | ||
| C£® | 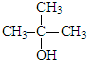 | D£® | 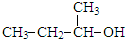 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com