
| A. | 80mL10mol/L的浓盐酸与足量MnO2反应,转移电子数为0.4 NA | |
| B. | 标准状况下,22.4LNO和11.2L氧气混合,气体的分子总数为1.5 NA | |
| C. | 7.2 g CaO2晶体中阴离子和阳离子总数为0.3 NA | |
| D. | 将1 mol NH4NO3溶于稀氨水中使溶液呈中性,溶液中NH4+数目为NA |
分析 A、二氧化锰只能和浓盐酸反应,和稀盐酸不反应;
B、NO和氧气混合后生成NO2,而NO2中存在平衡:NO2?2N2O4;
C、求出过氧化钙的物质的量,然后根据过氧化钙由1个钙离子和1个过氧根构成来分析;
D、将1 mol NH4NO3溶于稀氨水中使溶液呈中性,则有n(NH4+)=n(NO3-),根据电荷守恒来分析.
解答 解:A、二氧化锰只能和浓盐酸反应,和稀盐酸不反应,故反应不能进行彻底,则转移的电子数小于0.4NA个,故A错误;
B、NO和氧气混合后生成NO2,而NO2中存在平衡:NO2?2N2O4,导致分子个数减小,故小于1.5NA个,故B错误;
C、7.2g过氧化钙的物质的量为0.1mol,而过氧化钙由1个钙离子和1个过氧根构成,故0.1mol过氧化钙中含0.2NA个离子,故C错误;
D、将1 mol NH4NO3溶于稀氨水中使溶液呈中性,则有n(H+)=n(OH-),根据电荷守恒可知:n(NH4+)+n(H+)=n(NO3-)+n(OH-),故有n(NH4+)=n(NO3-)=1mol,故铵根离子的个数为NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.


科目:高中化学 来源: 题型:实验题
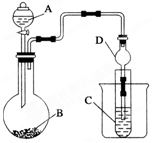 为探究元素的非金属性的变化规律,某化学兴趣小组同学设计了如下一系列实验,利用如图所示装置:
为探究元素的非金属性的变化规律,某化学兴趣小组同学设计了如下一系列实验,利用如图所示装置:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
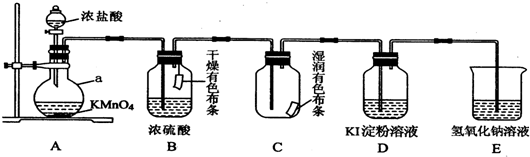
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 漂白粉、Cl2、氨水、NaHCO3 | B. | 福尔马林、苯、Cu2(OH)2CO3、明矾 | ||
| C. | 盐酸、SO2、纯碱、NH4Cl | D. | 食醋、C2H5OH、苛性钾、NaHSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑧ | B. | ①②⑤⑧ | C. | ②③⑦ | D. | ②⑥⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
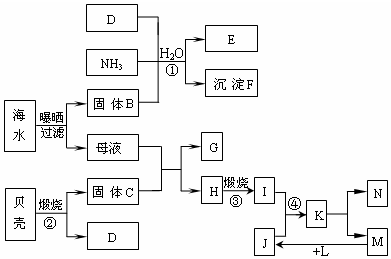
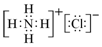 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 17g NH3含有电子数为10NA | |
| B. | 标况下,4.48LH2O中所含的分子数是0.2NA | |
| C. | 0.1mol/L的K2SO4溶液中,K+的数目为0.2NA | |
| D. | 30 g乙烷(C2H6)所含的原子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的处理具有重要意义.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | V甲=V乙>V丙 | B. | V丙>V乙>V甲 | C. | V乙>V丙>V甲 | D. | V甲=V乙=V丙 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com