
| A. | 溶液中的c(OH-)为1×10-10mol/L | |
| B. | 溶液中的c(H+)为1×10-4mol/L | |
| C. | 溶液中由水电离出来的c(OH-)为1×10-10mol/L | |
| D. | 溶液中由水电离出来的H+的浓度为1×10-4mol/L |
分析 A、1mL0.1mol/L的H2SO4溶液中c(H+)=0.2mol/L,稀释成2L溶液,氢离子浓度为10-4mol/L,根据Kw=c(H+)•c(OH-)=10-14计算c(OH-);
B、1mL0.1mol/L的H2SO4溶液中c(H+)=0.2mol/L,根据稀释定律,稀释前后氢离子的物质的量不变,据此计算稀释后溶液中的c(H+);
C、溶液中氢氧根离子是水电离出的,结合A的计算判断;
D、溶液中水电离出的氢离子浓度等于溶液中氢氧根离子浓度.
解答 解:A、1mL0.1mol/L的H2SO4溶液中c(H+)=0.2mol/L,稀释成2L溶液,溶液中氢离子浓度为$\frac{1{0}^{-3}L×0.2mol/L}{2L}$=10-4mol/L,所以溶液中c(OH-)=$\frac{1{0}^{-14}}{1{0}^{-4}}$mol/L=10-10mol/L,故A正确;
B、1mL0.1mol/L的H2SO4溶液中c(H+)=0.2mol/L,稀释成2L溶液,溶液中氢离子浓度为$\frac{1{0}^{-3}L×0.2mol/L}{2L}$=10-4mol/L,故B正确;
C、溶液中氢氧根离子是水电离出的,由A中计算可知溶液中c(OH-)=10-10mol/L,故C正确;
D、溶液中水电离出的氢离子浓度等于溶液中氢氧根离子浓度为10-10mol/L,故D错误.
故选D.
点评 本题考查物质的量浓度计算、溶液pH的计算等,难度不大,A中注意酸(或碱)溶液稀释接近中性时应考虑水的电离.


科目:高中化学 来源: 题型:选择题
| A. | 放电时PbO2为正极,反应的离子方程式为:PbO2+4H++2e-+SO42-═PbSO4+2H2O | |
| B. | 充电时Pb电极为阴极,反应的离子方程式为:PbSO4+2e-═Pb+SO42- | |
| C. | 放电时电解质溶液密度不断减小,可根据电解液密度来判断是否需要充电 | |
| D. | 充电时可直接使用交流电源,不需要充电器也可充入 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
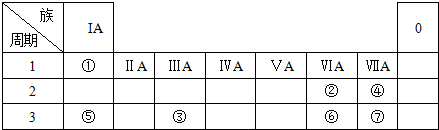
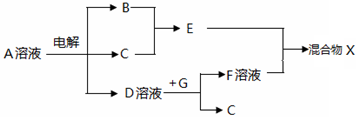
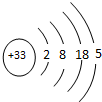 ,
,查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)25℃时,pH=2的某酸HnA(A为酸根)与pH=12的某碱B(OH)m等体积混合,混合液的pH变为6.生成的正盐中存在着一定水解的离子,该离子水解的离子方程式为An-+H2O?HA(n-1)-+OH-.
(1)25℃时,pH=2的某酸HnA(A为酸根)与pH=12的某碱B(OH)m等体积混合,混合液的pH变为6.生成的正盐中存在着一定水解的离子,该离子水解的离子方程式为An-+H2O?HA(n-1)-+OH-.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10.0mol•L-1 | B. | 16.0 mol•L-1 | C. | 12.4mol•L-1 | D. | 18.7mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
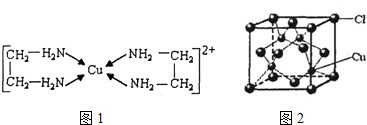
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 20℃ | K2CO3 | KHCO3 | K2SO4 | KMnO4 |
| s(g/100g水) | 111 | 33.7 | 11.1 | 6.34 |
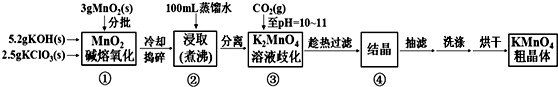
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com