
分析 W、X、Y、Z是周期表前36号元素中的四种常见元素,W、Y的氧化物是导致酸雨的主要物质,而导致酸雨的主要物质是二氧化氮和二氧化硫,Y的原子序数大于W的,所以W是N元素,Y是S元素;X的氧化物和氢氧化物都是两性物质,则X为Al;Z能形成红色(或砖红色)的Z2O和黑色的ZO两种氧化物,且Z是前36号元素,所以Z是铜元素,据此解答.
解答 解:W、X、Y、Z是周期表前36号元素中的四种常见元素,W、Y的氧化物是导致酸雨的主要物质,而导致酸雨的主要物质是二氧化氮和二氧化硫,Y的原子序数大于W的,所以W是N元素,Y是S元素;X的氧化物和氢氧化物都是两性物质,则X为Al;Z能形成红色(或砖红色)的Z2O和黑色的ZO两种氧化物,且Z是前36号元素,所以Z是铜元素.
(1)W为N元素,处于周期表中第二周期ⅤA族,由于非金属性N<O,故但的气态氢化物稳定性比H2O(g)弱,
故答案为:二、ⅤA;弱;
(2)Y为硫元素,硫原子核外电子数为16,基态核外电子排布式为1s22s22p63s23p4,Y的一种氧化物SO2能使品红溶液褪色的性质被称为漂白性,
故答案为:1s22s22p63s23p4;漂白;
(3)浓硫酸和铜在加热条件下能反应生成硫酸铜、水和二氧化硫,方程式为:2H2SO4(浓)+Cu$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,
故答案为:2H2SO4(浓)+Cu$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
(4)已知:①、Fe(s)+$\frac{1}{2}$O2(g)=FeO(s)△H=-272.0kJ•mol-1
②、2Al(s)+$\frac{3}{2}$O2(g)=Al2O3(s)△H=-1675.7kJ•mol-1
将方程式②-①×3得:3FeO(s)+2Al(s)=Al2O3(s)+3Fe(s)?△HH=-859.7KJ/mol
故答案为:3FeO(s)+2Al(s)=Al2O3(s)+3Fe(s)?△H=-859.7KJ/mol.
点评 本题考查了元素的推断、核外电子排布、热化学方程式等知识点,难度不大,能正确判断各元素是解本题的关键,注意书写基态原子核外电子排布式要遵循构造原理.


科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 LCCl4含有的分子数为NA | |
| B. | 1L0.1 mol•L-1 Na2CO3溶液中含有CO32-数为0.1 NA | |
| C. | 常温常压下,18g水含有的分子数为 NA | |
| D. | 常温下,1mol Cl2与过量NaOH溶液反应,转移电子总数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
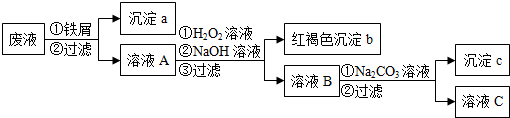
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 不同时间各物质的物质的量/mol | ||||
| 0min | 2min | 4min | 6min | |
| CH4 | 2.00 | 1.76 | 1.60 | n2 |
| H2 | 0.00 | 0.72 | n1 | 1.20 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烯能发生取代反应、加成反应,还能使酸性KMnO4溶液褪色 | |
| B. | 分子式为C7H16的烷烃,含有3个甲基的同分异构体有2种 | |
| C. | 甲苯中所有原子都处于同一平面 | |
| D. | 相同质量的甲烷和乙烷完全燃烧,乙烷耗氧量多 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
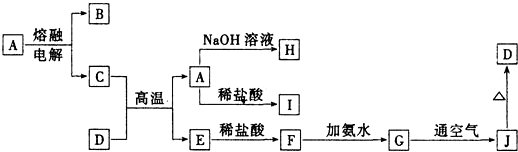
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
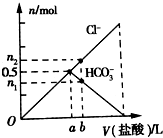 向Na2CO3溶液中逐滴滴加1mol•L-1盐酸,测得溶液中Cl-、HCO3-的物质的量随加入盐酸体积的关系如图所示,其中n2:n1=3:2,则下列说法不正确的是( )
向Na2CO3溶液中逐滴滴加1mol•L-1盐酸,测得溶液中Cl-、HCO3-的物质的量随加入盐酸体积的关系如图所示,其中n2:n1=3:2,则下列说法不正确的是( )| A. | 0a段反应的离子方程式为:CO32-+H+=HCO3- | |
| B. | 原Na2CO3溶液中含有0.5mol Na2CO3 | |
| C. | b点时生成的CO2的物质的量为0.1 mol | |
| D. | b点时HCO3-物质的量为0.6mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com