
已知某元素+2价离子的电子排布式为1s22s22p63s23p6,该元素在周期表中属于( )
A.ⅤB族 B.ⅡB族 C.Ⅷ族 D.ⅡA族
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
某溶液可能含有Cl-、SO 、CO
、CO 、NH
、NH 、Fe3+、Al3+和K+。取该溶液100 mL,加入过量NaOH溶液,加热,得到0.02 mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6 g固体;向上述滤液中加足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀。由此可知原溶液中 ( )
、Fe3+、Al3+和K+。取该溶液100 mL,加入过量NaOH溶液,加热,得到0.02 mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6 g固体;向上述滤液中加足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀。由此可知原溶液中 ( )
A.至少存在5种离子
B.Cl-一定存在,且c(Cl-)≥0.4 mol·L-1
C.SO 、NH
、NH 一定存在,Cl-可能不存在
一定存在,Cl-可能不存在
D.CO 、Al3+一定不存在,K+可能存在
、Al3+一定不存在,K+可能存在
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是( )
A.Fe与盐酸反应制H2:2Fe+6H+===2Fe3++3H2↑
B.用石墨电极电解饱和食盐水:2H++2Cl- Cl2↑+H2↑
Cl2↑+H2↑
C.用AlCl3和氨水制备Al(OH)3:Al3++3OH-===Al(OH)3↓
D.向Mg(OH)2浊液中滴入FeCl3溶液:3Mg(OH)2+2Fe3+2Fe(OH)3+3Mg2+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于晶体的说法,一定正确的是 ( )。
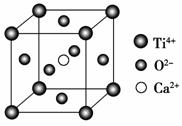
CaTiO3的晶体结构模型(图中Ca2+、O2-、
Ti4+分别位于立方体的体心、面心和顶角)
A.分子晶体中都存在共价键
B.如上图,CaTiO3晶体中每个Ti4+和12个O2-相紧邻
C.SiO2晶体中每个硅原子与两个氧原子以共价键相结合
D.金属晶体的熔点都比分子晶体的熔点高
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。

(1)请写出元素d的基态原子电子排布式________________________________________________________________________。
(2)b元素的氧化物中b与氧元素之间的共价键类型是________。其中b原子的杂化方式是________。
(3)a单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。

若已知a的原子半径为d,NA代表阿伏加德罗常数,a的相对原子质量为Mr,则一个晶胞中a原子的数目为________,该晶体的密度为________(用字母表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
元素的原子半径在周期表中呈现周期性变化的根本原因是( )
A.原子的相对原子质量呈现周期性变化
B.元素的化合价呈现周期性变化
C.原子的性质呈现周期性变化
D.元素原子的核外电子排布呈周期性变化
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、M是元素周期表中前20号元素,其原子序数依次增大,且X、Y、Z相邻。X的核电荷数是Y的核外电子数的一半,Y与M可形成化合物M2Y。下列说法正确的是( )
A.还原性:X的氢化物>Y的氢化物>Z的氢化物
B.简单离子的半径:M的离子>Z的离子>Y的离子>X的离子
C.YX2、M2Y都是含有极性键的极性分子
D.Z元素的最高价氧化物的水化物的化学式为HZO4
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,不符合ⅦA族元素性质特征的是( )
A.从上到下原子半径逐渐减小
B.易形成-1价离子
C.从上到下单质的氧化性逐渐减弱
D.从上到下氢化物的稳定性依次减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
已知1 g氢气完全燃烧生成液态水时放出热量143 kJ,18 g水蒸气变成液态水放出44 kJ的热量。其他相关数据如下表:
| O===O(g) | H—H | H—O | |
| 1 mol化学键断裂时需要吸收的能量/kJ | 496 | x | 463 |
则表中x为( )
A.920 B.557
C.436 D.188
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com