
| A. | 吸烟有害健康 | |
| B. | 尼古丁中C、H、N三种元素的质量比为5:7:1 | |
| C. | CO比O2更易同血红蛋白结合,会导致人体缺氧 | |
| D. | 尼古丁中氮元素的质量分数约为17.3% |
分析 A、尼古丁、CO等均对人体有害;
B、尼古丁中各种原子的质量=相对原子质量×个数;
C、CO易与人体中的血红蛋白结合;
D、元素质量分数=$\frac{原子质量}{物质质量}$.
解答 解:A、香烟燃烧产生的烟气中含有多种致癌物质和有害物质,吸烟有害健康,故A正确;
B、尼古丁中C、H、N的元素质量比为:(10×12):(1×14):(2×7)=60:7:14,故B错误;
C、CO易与人体中的血红蛋白结合,导致人体缺氧,故C正确;
D、氮元素的质量分数=$\frac{2×14}{10×12+1×14+2×14}$×100%=17.3%,故D正确,
故选B.
点评 本题主要考查的是元素质量分数的计算、化学式的含意等,难度不大.


 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:选择题
| A. | 滴入酚酞试液显红色的溶液中:K+、Na+、Cu2+、SO42- | |
| B. | 在$\frac{c({H}^{+})}{c(O{H}^{-})}$=10-12的溶液中:K+、Ba2+、Cl-、ClO- | |
| C. | 水电离产生的c(H+)=10-13mol•L-1 的溶液中:Na+、Cl-、NO3-、CH3COO- | |
| D. | pH=0的溶液中:Na+、NO3-、S2-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl、CuSO4、Mg(NO3)2、KOH | B. | NaBr、AgNO3、HCl、Na2CO3 | ||
| C. | H2SO4、NaCl、Na2SO4、Na2CO3 | D. | NaOH、(NH4)2CO3、Na2CO3、KHSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
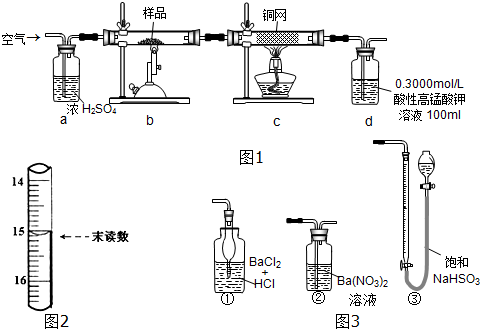
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 控制工业废水的排放 | B. | 控制生活污水的排放 | ||
| C. | 对被污水污染了的河流进行治理 | D. | 减少用水量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 维生素C具有还原性,在人体内起抗氧化作用 | |
| B. | 糖类、蛋白质、油脂属于天然高分子化合物 | |
| C. | 煤经气化和液化两个物理变化过程,可变为清洁能源 | |
| D. | 明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的消毒净化 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1 mol Fe溶解于一定量的HN03溶液中,电子转移数介于2NA和3NA间 | |
| B. | L mol FeCl3完全水解转化为氢氧化铁胶体后能生成NA个Fe(OH)3胶粒 | |
| C. | 0.01 mol Mg在空气中完全燃烧生成MgO和Mg3N2,转移电子数目为0.02NA | |
| D. | 10 mL 5mol/L (NH4)2S04溶液中含有NH4+数目为0.1NA个 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com