
分析 (1)浓硝酸性质不稳定,见光、受热易分解生成二氧化氮、氧气和水;
(2)氯化铵受热分解生成氨气和氯化氢.
解答 解:(1)浓硝酸见光、受热易分解,分解的化学方程式为4HNO3(浓)$\frac{\underline{\;见光或受热\;}}{\;}$4NO2↑+O2↑+2H2O,应保存在棕色试剂瓶中,放置在阴凉处,
故答案为:4HNO3(浓)$\frac{\underline{\;见光或受热\;}}{\;}$4NO2↑+O2↑+2H2O;
(2)氯化铵受热分解生成氨气和氯化氢,反应的化学方程式为:NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+HCl↑,
故答案为:NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+HCl↑.
点评 本题考查了化学方程式书写方法,侧重氮的化合物性质的考查,主要是物质性质和反应条件的理解应用,掌握基础是关键,题目较简单.


科目:高中化学 来源: 题型:实验题
 | 30% H2O2 | 15% H2O2 | 10% H2O2 | 5%H2O2 |
| 无催化剂、不加热 | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
| 无催化剂、加热 | 360 | 480 | 540 | 720 |
| 有催化剂、不加热 | 10 | 25 | 60 | 120 |
| 实验操作 | MnO2状态 | 观察结果 | 反应所需时间 |
| 将MnO2加入5mL5%过氧化氢溶液中,不震荡 | 粉末状 | 剧烈反应,带火星的木条复燃 | 3.5分钟 |
| 块状 | 反应较慢,火星红亮但木条未复燃 | 30分钟 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3-CH═CH-CH2-CH3 | B. | CH2═CH-CH═CH2 | ||
| C. | CH3═CH-CH3 | D. | CH3-CH═CH-CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②④ | C. | ③④ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10种 | B. | 12种 | C. | 14种 | D. | 16种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 厨房中用的食盐、食醋都是电解质 | |
| B. | 石油的分馏、煤的干馏、石油的裂解都是化学变化 | |
| C. | 工业上通过电解熔融的氯化物制取Na、Mg、Al三种金属 | |
| D. | 石油裂化的主要目的是为了提高轻质油的质量和产量 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用过滤的方法可以分离出溶液与胶体 | |
| B. | 在江河入海口处易形成沙洲 | |
| C. | 一束平行光线照射蛋白质溶液时从侧面可以看到一束光亮的通路 | |
| D. | 三氯化铁溶液中滴加氢氧化钠溶液出现氢氧化铁的胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
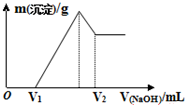 将0.1mol的镁、铝混合物溶于100mL 2mol/L H2SO4溶液中,然后再滴加1mol/L NaOH溶液.在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如图所示.下列说法不正确的是( )
将0.1mol的镁、铝混合物溶于100mL 2mol/L H2SO4溶液中,然后再滴加1mol/L NaOH溶液.在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如图所示.下列说法不正确的是( )| A. | O~V1发生反应的离子方程式为:H++OH-═H2O | |
| B. | 当V1=160mL时,V2的体积为360mL | |
| C. | 当V1=160mL时,金属混合物中镁的质量为1.44g | |
| D. | 当Mg2+、Al3+刚好沉淀完全,则滴入的NaOH溶液的体积为400mL |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
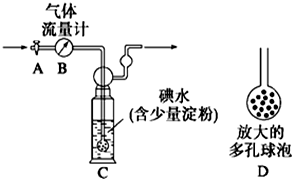
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com