
 ČēĶ¼ŹĒŅ»øö»Æѧ¹ż³ĢµÄŹ¾ŅāĶ¼£¬ŅŃÖŖ³ŲµÄ×Ü·“Ó¦Ź½ĪŖ2CH3OH+3O2+4KOHØT2K2CO3+6H2O£®
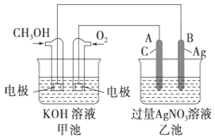
ČēĶ¼ŹĒŅ»øö»Æѧ¹ż³ĢµÄŹ¾ŅāĶ¼£¬ŅŃÖŖ³ŲµÄ×Ü·“Ó¦Ź½ĪŖ2CH3OH+3O2+4KOHØT2K2CO3+6H2O£®·ÖĪö øł¾Ż·“Ó¦·½³ĢŹ½ÖŖ£¬¼××°ÖĆŹĒŅ»øöČ¼ĮĻµē³Ų£¬ĖłŅŌ¼×ŹĒ°Ń»ÆѧÄÜ×Ŗ±äĪŖµēÄܵÄ×°ÖĆ£¬ŹĒŌµē³Ų£»ŅŅÓŠĶā¼ÓµēŌ“£¬ĖłŅŌŹĒµē½ā³Ų£®øł¾Ż2CH3OH+3O2+4KOH=2K2CO3+6H2OÖŖ£¬CH3OH·¢ÉśŃõ»Æ·“Ó¦£¬ĖłŅŌøƵē¼«ŹĒøŗ¼«£¬·“Ó¦Ź½ĪŖ£ŗCH3OH-6e-+8OH-=2CO32-+6H2O£¬O2 ·¢Éś»¹Ō·“Ó¦£¬ĖłŅŌøƵē¼«ŹĒÕż¼«£¬·“Ó¦Ź½ĪŖ£ŗO2+2H2O+4e-=4OH-£»ŹÆÄ«ÓėŌµē³ŲµÄÕż¼«ĻąĮ¬£¬ĖłŅŌŹÆÄ«µē¼«AŹĒŃō¼«Ź§µē×Ó·¢ÉśŃõ»Æ·“Ó¦£¬B¼«ĪŖŅõ¼«£¬ČÜŅŗÖŠµÄŅųĄė×ӵƵē×Ó·¢Éś»¹Ō·“Ó¦£¬¾Ż“Ė·ÖĪö½įŗĻµēĀ·ÖŠµĆŹ§µē×ÓŹŲŗć¼ĘĖć£®
½ā“š ½ā£ŗ£Ø1£©øł¾Ż·“Ó¦·½³ĢŹ½ÖŖ£¬¼××°ÖĆŹĒŅ»øöČ¼ĮĻµē³Ų£¬ĖłŅŌ¼×ŹĒŌµē³Ų£»øł¾Ż2CH3OH+3O2+4KOH=2K2CO3+6H2OÖŖ£¬¼×³ŲÖŠĻūŗÄĒāŃõ»Æ¼Ų£¬ŌņČÜŅŗµÄpH¼õŠ”£¬CH3OH·¢ÉśŃõ»Æ·“Ó¦£¬ĖłŅŌøƵē¼«ŹĒøŗ¼«£¬·“Ó¦Ź½ĪŖ£ŗCH3OH-6e-+8OH-=CO32-+6H2O£»¼×³ŲÖŠČÜŅŗµÄpH¹Ź“š°øĪŖ£ŗŌµē³Ų£»øŗ£»CH3OH-6e-+8OH-=CO32-+6H2O£»¼õŠ”£»
£Ø2£©ŅŅÓŠĶā¼ÓµēŌ“£¬ĖłŅŌŹĒµē½ā³Ų£¬ŹÆÄ«µē¼«AÓėŌµē³ŲµÄÕż¼«ĻąĮ¬£¬ĖłŅŌŹÆÄ«µē¼«AŹĒŃō¼«Ź§µē×Ó·¢ÉśŃõ»Æ·“Ó¦£¬·“Ó¦Ź½ĪŖ4OH--4e-=O2”ü+2H2O£»B¼«ĪŖŅõ¼«£¬ČÜŅŗÖŠµÄŅųĄė×ӵƵē×Ó·¢Éś»¹Ō·“Ó¦£¬×ܵķ“Ó¦Ź½£ŗ4AgNO3+2H2O$\frac{\underline{\;Ķصē\;}}{\;}$4Ag”ż+O2”ü+4HNO3£¬ŌņŅŅ³ŲÖŠČÜŅŗµÄpH¼õŠ”£»
¹Ź“š°øĪŖ£ŗµē½ā³Ų£»Ńō¼«£»¼õŠ”£»
£Ø3£©øł¾ŻµĆŹ§µē×ÓŹżĻąµČ£¬ŃõĘųÓėŅųµÄ¹ŲĻµŹ½ĪŖ£ŗ
O2--------4Ag
22.4L £Ø 4”Į108 £©g
280mL 5.40g
¹Ź“š°øĪŖ£ŗ280£®
µćĘĄ ±¾Ģāæ¼²éĮĖŌµē³ŲŗĶµē½ā³ŲµÄ¹¤×÷ŌĄķµÄÓ¦ÓĆ£¬Ö÷ŅŖæ¼²éĮĖŹĒµē³ŲÅŠ¶Ļ”¢µē¼«ÅŠ¶Ļ£¬µē½ā·½³ĢŹ½µÄŹéŠ“”¢µē×ÓŹŲŗćµÄÓ¦ÓĆµČ£¬ĢāÄæÄѶČÖŠµČ£®


 53ĖęĢĆ²āĻµĮŠ“š°ø
53ĖęĢĆ²āĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2.5mol | B£® | 4.5mol | C£® | 1.5mol | D£® | 0.6mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
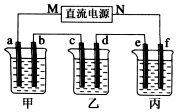 ČēĶ¼ĖłŹ¾×°ÖĆÖŠ£¬¼×”¢ŅŅ”¢±ūČżøöÉÕ±ŅĄ“Ī·Ö±šŹ¢·Å100g 5.00%µÄNaOHČÜŅŗ”¢×ćĮæµÄCuSO4ČÜŅŗŗĶ100g 10.00%µÄK2SO4ČÜŅŗ£¬µē¼«¾łĪŖŹÆÄ«µē¼«£®½ÓĶصēŌ“£¬¾¹żt mimŗ󣬲āµĆ¼×ÖŠNaOHÅضČĪŖ6.097%£¬ŅŅÖŠdµē¼«ÖŹĮæŌö¼Ó£®¾Ż“Ė»Ų“šĪŹĢā£ŗ
ČēĶ¼ĖłŹ¾×°ÖĆÖŠ£¬¼×”¢ŅŅ”¢±ūČżøöÉÕ±ŅĄ“Ī·Ö±šŹ¢·Å100g 5.00%µÄNaOHČÜŅŗ”¢×ćĮæµÄCuSO4ČÜŅŗŗĶ100g 10.00%µÄK2SO4ČÜŅŗ£¬µē¼«¾łĪŖŹÆÄ«µē¼«£®½ÓĶصēŌ“£¬¾¹żt mimŗ󣬲āµĆ¼×ÖŠNaOHÅضČĪŖ6.097%£¬ŅŅÖŠdµē¼«ÖŹĮæŌö¼Ó£®¾Ż“Ė»Ų“šĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na2CO3ČÜŅŗ£ØNaHCO3£©£¬¼ÓČČ | |
| B£® | Ģś·Ū£ØĀĮ·Ū£©£ŗ¼ÓČė¹żĮæµÄ°±Ė®ŗó¹żĀĖ | |
| C£® | NaClČÜŅŗ£ØNa2SO4£©£ŗ¼ÓČėŹŹĮæµÄĻõĖį±µŗó¹żĀĖ | |
| D£® | µķ·ŪČÜŅŗ£ØKCl£©£ŗĶعż°ėĶøĤ½ųŠŠÉųĪö |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÖŠŗĶ·Ø | B£® | Ńõ»Æ»¹Ō·Ø | C£® | ×ŌČ»³Į½µ·Ø | D£® | Ąė×Ó½»»»·Ø |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
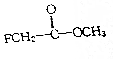 ·śŅŅĖį¼×·ÓŹōÓŚ¾ē¶¾»Æ¹¤Ę·£¬½Ó“„²»É÷ÓŠÖĀĆüĪ£ĻÕ£¬·śŅŅĖį¼×·ÓµÄ½į¹¹¼ņŹ½ČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©
·śŅŅĖį¼×·ÓŹōÓŚ¾ē¶¾»Æ¹¤Ę·£¬½Ó“„²»É÷ÓŠÖĀĆüĪ£ĻÕ£¬·śŅŅĖį¼×·ÓµÄ½į¹¹¼ņŹ½ČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | Ėüŗ¬ÓŠĮ½ÖÖ¹ŁÄÜĶÅ | B£® | ĖüŹōÓŚĀ±“śĢž | ||
| C£® | ĖüÄÜ·¢ÉśĖ®½ā·“Ó¦ | D£® | ĖüŹōÓŚĢžµÄŃÜÉśĪļ£® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÉŁĮæSO2ĶØČėCa£ØClO£©2ČÜŅŗÖŠ£ŗSO2+H2O+Ca2++2ClO-ØTCaSO3”ż+2HClO | |
| B£® | Fe£ØNO3£©3ČÜŅŗÖŠ¼ÓČĖ¹żĮæµÄHIČÜŅŗ2Fe3++2I-ØT2Fe2++I2 | |
| C£® | NaNO2ČÜŅŗÖŠ¼ÓČėĖįŠŌKMnO4ČÜŅŗ£ŗ2MnO4-+5NO2-+6H+ØT2Mn2++5NO3-+3H2O | |
| D£® | NaHCO3ČÜŅŗÖŠ¼ÓČė¹żĮæµÄBa£ØOH£©2ČÜŅŗ£ŗ2HCO3-+Ba-+2BaCO3”ż+2HO+CO32- |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com