
现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-、SO42-、和NO3-的相互分离。相应的实验过程可用下图表示: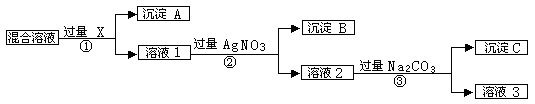
请回答下列问题:
⑴写出实验中下列物质的化学式:试剂X : ,沉淀A: ,沉淀B: 。
⑵上述实验流程中加入过量的Na2CO3的目是 。
⑶按此实验方案得到的溶液3中肯定含有 (填化学式)杂质;为了解决这个问题,可以向溶液3中加入适量的 ,之后若要获得固体NaNO3需进行的实验操作是 (填操作名称)。
(共10分)(1)BaCl2 或Ba(NO3 )2 BaSO4 AgCl (各1分)
(2)除去溶液中多余的Ba2+和Ag+ (2分) (3)Na2CO3 (1分) 硝酸 蒸发(各2分)
解析试题分析:(1)如先加入AgNO3,则会同时生成Ag2SO4和AgCl沉淀,则应先加入过量的BaCl2[或Ba(NO3)2],生成BaSO4沉淀,然后在滤液中加入过量的AgNO3,使Cl-全部转化为AgCl沉淀,则试剂X为BaCl2[或Ba(NO3)2],沉淀A为BaSO4,沉淀B为AgCl。
(2)加入过量的BaCl2[或Ba(NO3)2],然后在滤液中加入过量的AgNO3,使Cl-全部转化为AgCl沉淀,在所得滤液中含有Ag+、Ba2+,在所得滤液中加入过量的Na2CO3,使溶液中的Ag+、Ba2+完全沉淀。
(3)在所得滤液中加入过量的Na2CO3,最后所得溶液为NaNO3和Na2CO3的混合物,加入稀HNO3,最后进行蒸发操作可得固体NaNO3。
考点:考查物质的分离与提纯的有关判断
点评:该题是高考中的常见题型,属于中等难度的试题。题目难度中等,基础性强,侧重对学生能力的培养和解题方法的指导与训练。本题注意Cl-、SO42-的性质,把握除杂原则,提纯时不能引入新的杂质,注意把握实验的先后顺序等,有利于培养学生严谨、规范的实验设计和操作动手能力。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
| 实验步骤 | 预期现象和结论 |
| 步骤1:用量筒取样品溶液2mL于试管中,再滴加足量的2mol/L盐酸,充分振荡,观察 | 若 溶液由无色变黄色 溶液由无色变黄色 ,则假设1可能成立;若溶液无明显变化 溶液无明显变化 ,则假设2可能成立 假设2可能成立 . |
| 步骤2:往步骤1 的试管中加入 1mL苯 1mL苯 ,充分振荡,观察 |
若溶液分层,上层有机层出现橙色或橙红色,则假设2成立; 若溶液只分层,无颜色变化,则假设1成立 若溶液分层,上层有机层出现橙色或橙红色,则假设2成立; 若溶液只分层,无颜色变化,则假设1成立 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| m |
| M |
| m |
| M |
| 2mNA |
| M |
| 2mNA |
| M |
| 22.4m |
| M |
| 22.4m |
| M |
查看答案和解析>>
科目:高中化学 来源: 题型:022
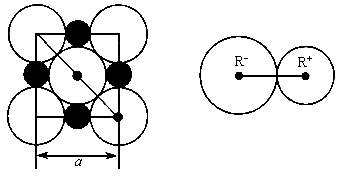
晶胞是晶体中最小重复单位,并在空间不断伸展构成晶体。NaCl晶体是一个正六面体(如图)。我们把阴、阳离子看成不等径的圆球,并彼此相切,离子键的键长是相邻阴阳离子的半径之和(如图)。已知a为常数,请计算下列问题:
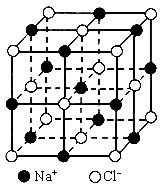
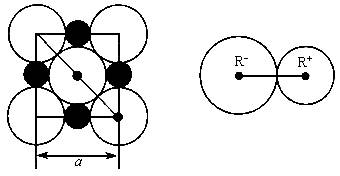
(1)每个晶胞中平均分摊________个Na+,________个Cl-;
(2)若某NaCl晶体的质量为5.85g,它约含________mol NaCl晶胞;
(3)NaCl晶体离子键的键长为________,Na+离子半径与Cl-离子半径之比为![]() ________;
________;
(4)NaCl晶体不存在分子,但在高温下(大于等于1413℃时)晶体转变成气体NaCl的分子形式存在,现有1mol NaCl晶体,加强热使其气化,测得气体体积为11.2L(已折为标准状况)。则此时氯化钠气体的分子式为________。
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:022
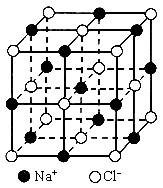
(1)每个晶胞中平均分摊________个Na+,________个Cl-;
(2)若某NaCl晶体的质量为5.85g,它约含________mol NaCl晶胞;
(3)NaCl晶体离子键的键长为________,Na+离子半径与Cl-离子半径之比为![]() ________;
________;
(4)NaCl晶体不存在分子,但在高温下(大于等于1413℃时)晶体转变成气体NaCl的分子形式存在,现有1mol NaCl晶体,加强热使其气化,测得气体体积为11.2L(已折为标准状况)。则此时氯化钠气体的分子式为________。
查看答案和解析>>
科目:高中化学 来源:知识精讲与能力训练 高三化学 题型:022
晶胞里晶体中最小重复单位,并在空间不断伸展构成晶体.NaCl晶体是一个正六面体(图参照例题).我们把阴、阳离子看成不等径的圆球,并彼此相切,离子键的键长是相邻阴阳离子的半径之和(如图).已知a为常数,请计算下列问题:
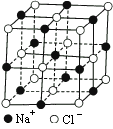
(1)每个晶胞中平均分摊________个Na+,________个Cl-.
(2)若某NaCl晶体的质量为5.85克,它约含________摩尔NaCl晶胞.
(3)NaCl晶体离子键的键长为________,Na+离子半径与Cl-离子半径之比为![]() =________.
=________.
(4)NaCl晶体不存在分子,但在高温下(≥1413℃时)晶体转变成气体NaCl的分子形式存在,现有1mol NaCl晶体,加强热使其气化,测得气体体积为11.2升(已折为标况).则此时氯化钠气体的分子式为________.
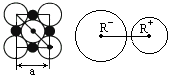
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com