
 计算49克硫酸的物质的量,根据c=
计算49克硫酸的物质的量,根据c= 计算溶液的物质的量浓度;溶液中n(H+)=nc(H2SO4),根据N=nNA计算氢离子数目;溶液中c(SO42-)=n(H2SO4),根据n=cV计算硫酸根的数目,再根据N=nNA计算硫酸根离子数目.
计算溶液的物质的量浓度;溶液中n(H+)=nc(H2SO4),根据N=nNA计算氢离子数目;溶液中c(SO42-)=n(H2SO4),根据n=cV计算硫酸根的数目,再根据N=nNA计算硫酸根离子数目.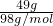 =0.5mol;
=0.5mol;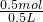 =1mol/L;
=1mol/L;

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫酸的摩尔质量为98g | B、11.7g NaCl的物质的量为0.2mol | C、1mol Na2CO3的质量为106g | D、16g CH4与4g H2的物质的量相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A.硫酸的摩尔质量为98 g
B.1 L 1 mol·L-1的氯化钙溶液中,Cl-的浓度为2 mol·L-1
C.若NA表示阿伏加德罗常数的值,则标准状况下11.2 L H2所含氢原子数为NA
D.从1 mol· L-1的NaCl溶液中倒出5 mL溶液,Na+的浓度为1 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2012-2013学年辽宁省沈阳市皇姑区实验中学高一(上)月考化学试卷(10月份)(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com