
| c |
| t |


科目:高中化学 来源: 题型:
| 1 |
| 27 |
| 1 |
| 27 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A.方程式中x=4
B.达到平衡时,A、B两反应物的转化率之比为α(A):α(B)=3:1
C.若继续向原平衡混合物的容器中通入少量氦气(氦气和A、B、C都不反应)后,正逆反应的化学反应速率变小
D.在t℃时,若向原平衡混合物的容器中再充入amolC,欲使达到新的平衡时,各物质的物质的量分数与原平衡相同,则应再充入a/4molB
查看答案和解析>>
科目:高中化学 来源:2013届辽宁省沈阳二中高三第四次阶段测试化学试卷(带解析) 题型:填空题
(10分) t℃时,将3mol A和1mol B气体通入容积为2L的密闭容器中(容积不变),发生如下反应3A(g)+B(g)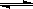 xC(g),2min时反应到达平衡状态(温度不变),此时容器内剩余了0.8mol B,并测得C的浓度为0.4mol·L-1。请填写下列空白:
xC(g),2min时反应到达平衡状态(温度不变),此时容器内剩余了0.8mol B,并测得C的浓度为0.4mol·L-1。请填写下列空白:
(1)从反应开始到平衡状态,生成C的平均反应速率为____________________。
(2) x = ____。
(3)若向原平衡混合物的容器中再充入a molC, 在t℃时达到新的平衡,此时B的物质的量为n(B) = ___________mol。(用含a的代数式表示)
(4)保持温度和容积不变,对原平衡混合物中三者的物质的量作如下调整,可使平衡向右移动的是______(填字母)。
A.均减半 B.均加倍 C.均增加0.4 mol D.均减少0.4 mol
(5)如果上述反应在相同温度和容积的容器中进行,起始加入3 molA和3mol B,达到平衡时A的体积分数为a%。其它条件不变时,按下列配比作为起始物质,平衡时A的体积分数大于a%的是 (填字母)。
A.2 molC B.1molA、3molB和4molC
C.1mol B和4molC D.6molA和2molB
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com