
| A、124g P4含有P-P键的个数为4NA |
| B、12g石墨中含有C-C键的个数为3NA |
| C、12g金刚石中含有C-C键的个数为2NA |
| D、60g SiO2中含Si-O键的个数为2NA |
| 1 |
| 2 |
| 3 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |
| 1 |
| 2 |


科目:高中化学 来源: 题型:
| 编组 | 强电解质 | 弱电解质 | 非电解质 |
| A | NaCl | HF | Cl2 |
| B | H2SO4 | BaCO3 | CO2 |
| C | AgCl | HClO | Cu |
| D | Ba(OH)2 | H2S | 蔗糖 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 A-M有如图转化关系.已知D、L是相对分子质量相等的两种气体,且含有同一种元素,D是石油化工的重要基础原料,也是一种植物生长调节剂;A、E都是无色溶液,B是无色气体单质,反应②、③、④都是工业生产中的重要反应,H与J反应生成的溶液遇苯酚显紫色.(有些反应条件已省略)
A-M有如图转化关系.已知D、L是相对分子质量相等的两种气体,且含有同一种元素,D是石油化工的重要基础原料,也是一种植物生长调节剂;A、E都是无色溶液,B是无色气体单质,反应②、③、④都是工业生产中的重要反应,H与J反应生成的溶液遇苯酚显紫色.(有些反应条件已省略)查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | E | F | |
| 主要化合价 | -1 | -3+5 | -2+6 | -1+7 | +2 | +1+2 |
| 原子半径 | 0.071 | 0.11 | 0.102 | 0.099 | 0.197 | 0.117 |

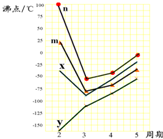
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:1 | B、2:1 |
| C、1:2 | D、3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、36g镁在足量的氮气中完全燃烧共转移的电子数为3NA |
| B、常温下,1L 0.1mol/L的NH4NO3溶液中含氮原子数为0.2NA |
| C、标准状况下,44.8 L NO与22.4 LO2混合后气体中分子总数为3NA |
| D、1 molNa2O和Na2O2混合物中含有的阴、阳离子总数是3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com