
”¾ĢāÄæ”æøł¾Żµē»ÆѧÖŖŹ¶»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ČēĶ¼ĖłŹ¾£¬ŌŚ²»Ķ¬µÄµē½āÖŹČÜŅŗÖŠæÉŅŌ×é³É²»Ķ¬µÄµē³Ų”£

¢Łµ±µē½āÖŹČÜŅŗĪŖĻ”ĮņĖįŹ±£¬Feµē¼«ŹĒ________(Ģī”°Õż”±»ņ”°øŗ”±)¼«,Ęäµē¼«·“Ó¦Ź½ĪŖ__________”£
¢Śµ±µē½āÖŹČÜŅŗĪŖNaOHČÜŅŗŹ±£¬Alµē¼«ŹĒ________(Ģī”°Õż”±»ņ”°øŗ”±) ¼«£¬Ęäµē¼«·“Ó¦Ź½ĪŖ_________”£
¢ŪČō°ŃĀĮøÄĪŖŠæ£¬µē½āÖŹČÜŅŗĪŖÅØĻõĖį£¬ŌņFeµē¼«ŹĒ______(Ģī”°Õż”±»ņ”°øŗ”±)¼«£¬Ęäµē¼«·“Ó¦Ź½ĪŖ_______________________________”£
£Ø2£©ĒėÄćĄūÓĆŌµē³ŲŌĄķ£¬Éč¼ĘŹµŃ飬±Č½ĻĶŗĶŅųµÄ½šŹō»ī¶ÆŠŌ”£»³öŹµŃé×°ÖĆĶ¼£¬±ź³öÕżøŗ¼«”¢µē×ÓĮ÷¶Æ·½Ļņ”£________

”¾“š°ø”æ Õż 2H£«£«2e£===H2”ü øŗ Al£3e££«4OH£===AlO![]() £«2H2O Õż NO
£«2H2O Õż NO![]() £«2H£«£«e£===NO2”ü£«H2O
£«2H£«£«e£===NO2”ü£«H2O 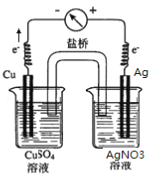
”¾½āĪö”æŹŌĢā·ÖĪö£ŗ£Ø1£©¢ŁĀĮµÄ»īĘĆŠŌ“óÓŚĢś£¬µ±µē½āÖŹČÜŅŗĪŖĻ”ĮņĖįŹ±£¬ĀĮŹĒøŗ¼«”¢ĢśŹĒÕż¼«£»¢ŚĀĮÄÜÓėĒāŃõ»ÆÄĘ·“Ó¦£¬µ±µē½āÖŹČÜŅŗĪŖNaOHČÜŅŗŹ±£¬ĀĮŹĒøŗ¼«£»¢ŪČō°ŃĀĮøÄĪŖŠæ£¬µē½āÖŹČÜŅŗĪŖÅØĻõĖį£¬ĢśŌŚÅØĻõĖįÖŠ¶Ū»Æ£¬ĢśŹĒÕż¼«£»(2)ĄūÓĆŌµē³ŲŌĄķ£¬±Č½ĻĶÓėŅųµÄ½šŹō»ī¶ÆŠŌĒæČõ£¬Ķ×öŌµē³ŲµÄøŗ¼«£¬Ņų×öÕż¼«£¬°ŃĶ²åŌŚĮņĖįĶČÜŅŗÖŠ£¬Ņų²åČėĻõĖįŅųČÜŅŗÖŠ£¬ÓƵ¼ĻßĮ¬½Ó£¬Į½øöÉÕ±ÓĆŃĪĒÅĮ¬½Ó£¬µē×ÓÓÉĶ¾µ¼ĻßĮ÷ĻņŅų£»
½āĪö£ŗ£Ø1£©¢ŁĀĮµÄ»īĘĆŠŌ“óÓŚĢś£¬µ±µē½āÖŹČÜŅŗĪŖĻ”ĮņĖįŹ±£¬ĀĮŹĒøŗ¼«”¢ĢśŹĒÕż¼«£¬Õż¼«ĒāĄė×ӵƵē×ÓÉś³ÉĒāĘų£¬µē¼«·“Ó¦Ź½ŹĒ2H£«£«2e£===H2”ü£»¢ŚĀĮÄÜÓėĒāŃõ»ÆÄĘ·“Ó¦£¬µ±µē½āÖŹČÜŅŗĪŖNaOHČÜŅŗŹ±£¬ĀĮŹĒøŗ¼«£¬øŗ¼«ĀĮŹ§µē×ÓÉś³ÉAlO![]() £¬øŗ¼«·“Ó¦Ź½ŹĒAl£3e££«4OH£===AlO
£¬øŗ¼«·“Ó¦Ź½ŹĒAl£3e££«4OH£===AlO![]() £«2H2O£»¢ŪČō°ŃĀĮøÄĪŖŠæ£¬µē½āÖŹČÜŅŗĪŖÅØĻõĖį£¬ĢśŌŚÅØĻõĖįÖŠ¶Ū»Æ£¬ĢśŹĒÕż¼«£¬Õż¼«NO
£«2H2O£»¢ŪČō°ŃĀĮøÄĪŖŠæ£¬µē½āÖŹČÜŅŗĪŖÅØĻõĖį£¬ĢśŌŚÅØĻõĖįÖŠ¶Ū»Æ£¬ĢśŹĒÕż¼«£¬Õż¼«NO![]() µĆµē×ӷųöNO2ĘųĢå£¬Õż¼«·“Ó¦Ź½ŹĒNO
µĆµē×ӷųöNO2ĘųĢå£¬Õż¼«·“Ó¦Ź½ŹĒNO![]() £«2H£«£«e£===NO2”ü£«H2O£»(2)ĄūÓĆŌµē³ŲŌĄķ£¬±Č½ĻĶÓėŅųµÄ½šŹō»ī¶ÆŠŌĒæČõ£¬Ķ×öŌµē³ŲµÄøŗ¼«£¬Ņų×öÕż¼«£¬°ŃĶ²åŌŚĮņĖįĶČÜŅŗÖŠ£¬Ņų²åČėĻõĖįŅųČÜŅŗÖŠ£¬ÓƵ¼ĻßĮ¬½Ó£¬Į½øöÉÕ±ÓĆŃĪĒÅĮ¬½Ó£¬µē×ÓÓÉĶ¾µ¼ĻßĮ÷ĻņŅų£»×°ÖĆĶ¼ĪŖ
£«2H£«£«e£===NO2”ü£«H2O£»(2)ĄūÓĆŌµē³ŲŌĄķ£¬±Č½ĻĶÓėŅųµÄ½šŹō»ī¶ÆŠŌĒæČõ£¬Ķ×öŌµē³ŲµÄøŗ¼«£¬Ņų×öÕż¼«£¬°ŃĶ²åŌŚĮņĖįĶČÜŅŗÖŠ£¬Ņų²åČėĻõĖįŅųČÜŅŗÖŠ£¬ÓƵ¼ĻßĮ¬½Ó£¬Į½øöÉÕ±ÓĆŃĪĒÅĮ¬½Ó£¬µē×ÓÓÉĶ¾µ¼ĻßĮ÷ĻņŅų£»×°ÖĆĶ¼ĪŖ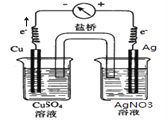 ”£
ӣ



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆ98%µÄÅØH2SO4£ØĆܶČĪŖ1.84g/mL£©ÅäÖĘ1molL©1µÄĻ”H2SO4 100mL£¬ÅäÖĘ¹ż³ĢÖŠæÉÄÜÓƵ½ĻĀĮŠŅĒĘ÷£ŗ¢Ł100mLĮæĶ²£»¢Ś10mLĮæĶ²£»¢Ū50mLÉÕ±£»¢ÜĶŠÅĢĢģĘ½£»¢Ż100mLČŻĮæĘ棻 ¢Ž½ŗĶ·µĪ¹Ü£»¢ß²£Į§°ō£®°“Ź¹ÓĆ³öĻÖµÄĻČŗóĖ³ŠņÅÅĮŠÕżČ·µÄŹĒ£Ø £©
A.¢Ś¢Ž¢Ū¢ß¢Ż
B.¢Ü¢Ū¢Ż¢ß¢Ž
C.¢Ł¢Ū¢ß¢Ż¢Ž
D.¢Ś¢Ż¢ß¢Ž
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŹµŃéŹŅÓŠČżĘæŹ§Č„±źĒ©µÄŹŌ¼Į£¬·Ö±šŹĒNa2CO3”¢NaCl”¢AgNO3”£ŹµŃéŌ±Ń”ŌńĮĖŅ»ÖÖŹŌ¼ĮÓĆ»Æѧ·½·ØŅ»“ĪŠŌ¾Ķ°ŃĖüĆĒĒų±šæŖĄ“ĮĖ£¬ÕāÖÖŹŌ¼ĮŹĒ£ŗ£Ø £©
A. ŃĪĖį B. ĒāŃõ»ÆÄĘČÜŅŗ C. ĀČ»Æ±µČÜŅŗ D. ĻõĖį
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ³£ĪĀĻĀ£¬ÓĆ0.1molL©1 NaOHČÜŅŗµĪ¶Ø20mL 0.1molL©1CH3COOHČÜŅŗµÄµĪ¶ØĒśĻßČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £© 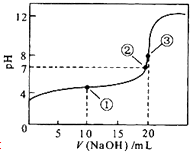
A.µć¢ŁĖłŹ¾ČÜŅŗÖŠ£ŗc£ØNa+£©£¾c£ØCH3COO©£©£¾c£ØCH3COOH£©£¾c£ØH+£©£¾c£ØOH©£©
B.µć¢ŚĖłŹ¾ČÜŅŗÖŠ£ŗc£ØNa+£©+c£ØH+£©=c£ØCH3COO©£©+c£ØCH3COOH£©+c£ØOH©£©
C.µć¢ŪĖłŹ¾ČÜŅŗÖŠ£ŗc£ØCH3COO©£©£¾c£ØNa+£©£¾c£ØOH©£©£¾c£ØH+£©
D.ŌŚÕūøöµĪ¶Ø¹ż³ĢÖŠ£ŗČÜŅŗÖŠ ![]() Ź¼ÖÕ²»±ä
Ź¼ÖÕ²»±ä
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijŌŖĖŲRµÄĀČ»ÆĪļČÜŅŗ10mL£¬ĘäÅضČĪŖ0.05mol/L£¬ÄÜĒ”ŗĆÓė0.1mol/LµÄ AgNO3ČÜŅŗ15mLĶźČ«·“Ó¦£¬ŌņRĀČ»ÆĪļµÄ»ÆѧŹ½ĪŖ
A. RCl B. RCl2 C. RCl3 D. RCl4
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĪĀ¶ČĻĀ£¬Č”Ņ»¶ØÖŹĮæµÄĮņĖįĶČÜŅŗ£¬ÓĆŹÆÄ«×öµē¼«½ųŠŠµē½ā£¬µ±Ńō¼«²śÉś±źæöĻĀĘųĢå1.12LŹ±£¬CuSO4Ē”ŗƱ»ĶźČ«µē½ā£¬µĆµ½ĆܶČĪŖ1.2gcm©3µÄČÜŅŗ200mL£®Ēó£ŗ
£Ø1£©Š“³öÓĆŹÆÄ«ĪŖµē¼«µē½āCuSO4ČÜŅŗµÄ»Æѧ·½³ĢŹ½ £®
£Ø2£©µē½āŗóĖłµĆČÜŅŗµÄpHĪŖ £®
£Ø3£©µē½āĒ°ĖłČ”CuSO4ČÜŅŗµÄÖŹĮæĪŖg£®
£Ø4£©ČōŅŖŹ¹µē½āŗóĖłµĆČÜŅŗ»Öø“ÖĮµē½āĒ°µÄŌדĢ¬£¬ŠčŅŖ¼ÓČėŗĪÖÖĪļÖŹ£ØÖ»ŅŖĒ󊓳öŅ»ÖÖ£©£¬Ęä»ÆѧŹ½ĪŖ £¬ ¼ÓČėĪļÖŹµÄÖŹĮæĪŖg£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A.Ē¦Šīµē³Ų·ÅµēŹ±Ē¦µē¼«·¢Éś»¹Ō·“Ó¦
B.µē½ā±„ŗĶŹ³ŃĪĖ®ŌŚŃō¼«µĆµ½ĀČĘų£¬Ņõ¼«µĆµ½½šŹōÄĘ
C.øųĢś¶¤¶ĘĶæɲÉÓĆCuSO4×÷µē¶ĘŅŗ
D.ÉśĢś½žÅŻŌŚŹ³ŃĪĖ®ÖŠ·¢ÉśĪöĒāøÆŹ“
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄ³Ń§Ļ°Š”×éÓĆČēĶ¼×°ÖĆ²ā¶ØĀĮĆ¾ŗĻ½šÖŠĀĮµÄÖŹĮæ·ÖŹżŗĶĀĮµÄĻą¶ŌŌ×ÓÖŹĮ森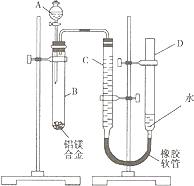
£Ø1£©AÖŠŹŌ¼ĮĪŖ £®
£Ø2£©ŹµŃéĒ°£¬ĻČ½«ĀĮĆ¾ŗĻ½šŌŚĻ”ĻõĖįÖŠ½žÅŻĘ¬æĢ£¬ĘäÄæµÄŹĒ £®
£Ø3£©¼ģ²éĘųĆÜŠŌ£¬½«Ņ©Ę·ŗĶĖ®×°Čėø÷ŅĒĘ÷ÖŠ£¬Į¬½ÓŗĆ×°ÖĆŗ󣬊č½ųŠŠµÄ²Ł×÷»¹ÓŠ£ŗ¢Ł¼ĒĀ¼CµÄŅŗĆęĪ»ÖĆ£»¢Ś½«BÖŠŹ£Óą¹ĢĢå¹żĀĖ”¢Ļ“µÓ”¢øÉŌļ£¬³ĘÖŲ£»¢Ū“żBÖŠ²»ŌŁÓŠĘųĢå²śÉś²¢»Öø“ÖĮŹŅĪĀŗ󣬼ĒĀ¼CµÄŅŗĆęĪ»ÖĆ£»¢ÜÓÉAĻņBÖŠµĪ¼Ó×ćĮæŹŌ¼Į£»¢Ż¼ģ²éĘųĆÜŠŌ£®ÉĻŹö²Ł×÷µÄĖ³ŠņŹĒ£ØĢīŠņŗÅ£©£»¼ĒĀ¼CµÄŅŗĆęĪ»ÖĆŹ±£¬³żŹÓĻßĘ½ŹÓĶā£¬»¹Ó¦ £®
£Ø4£©BÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ £®
£Ø5£©ČōŹµŃéÓĆĀĮĆ¾ŗĻ½šµÄÖŹĮæĪŖa g£¬²āµĆĒāĘųĢå»żĪŖb mL £ØŅŃ»»ĖćĪŖ±ź×¼×“æö£©£¬BÖŠŹ£Óą¹ĢĢåÖŹĮæĪŖc g£¬ŌņĀĮµÄĻą¶ŌŌ×ÓÖŹĮæĪŖ £®
£Ø6£©ŹµŃé¹ż³ĢÖŠ£¬ČōĪ“Ļ“µÓ¹żĀĖĖłµĆµÄ²»ČÜĪļ£¬Ōņ²āµĆĀĮµÄÖŹĮæ·ÖŹż½«£ØĢī”°Ę«“ó”±”¢”°Ę«Š””±”¢”°²»ŹÜÓ°Ļģ”±£©£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·ØÕżČ·µÄŹĒ £Ø £©
A. ĀČĘųŹĒ»ĘĀĢÉ«µÄ£¬C1”ŖŹĒĪŽÉ«µÄ
B. H2ŌŚC12ÖŠÄÜ°²¾²Č¼ÉÕ£¬»šŃę³Ź²Ō°×É«£¬ĘææŚÓŠ°×É«ŃĢĪķÉś³É
C. Cl2ŗĶH2µÄ»ģŗĻĘųŅ»¶Ø»į·¢Éś±¬ÕØ
D. Č¼ÉÕŹ±Ņ»¶ØŅŖÓŠŃõĘų²Ī¼Ó
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com