
| A.钢铁发生电化学腐蚀的正极反应式为:Fe-2e-=Fe2+ |
| B.氢氧燃料电池的负极反应式为:O2+2H2O+4e-=4OH- |
| C.粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-=Cu2+ |
| D.电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-=Cl2↑ |
科目:高中化学 来源:不详 题型:填空题
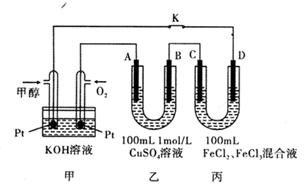
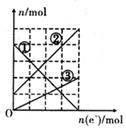
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
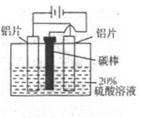
 3Zn+2K2FeO4+8H2O,该电池放电时正极材料的化学式是 其电极反应式是______,若电路中通过1.204×1023个电子时,负极质量变化为______g充电时,该电池的正极接直流电源的______(填“正极”或“负极”)。
3Zn+2K2FeO4+8H2O,该电池放电时正极材料的化学式是 其电极反应式是______,若电路中通过1.204×1023个电子时,负极质量变化为______g充电时,该电池的正极接直流电源的______(填“正极”或“负极”)。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
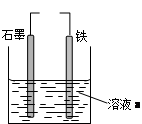
| A.若两电极直接连接,a是食盐水,则发生析氢腐蚀 |
| B.若两电极直接连接,则电子从铁流向石墨 |
| C.若铁接电源负极,石墨接电源正极,a是稀H2SO4溶液,电解一段时间后溶液的pH增大 |
| D.若铁接电源正极,石墨接电源负极,a是氯化铜溶液,阴离子向石墨电极移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.破损的镀锌铁在潮湿的空气中更易被腐蚀 |
| B.金属腐蚀就是金属原子失去电子被还原的过程 |
| C.当镀锡铁制品的镀层破损时,锡层仍能对铁制品起保护作用 |
| D.在海轮外壳连接锌块保护外壳不受腐蚀是采用了电化学保护法 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
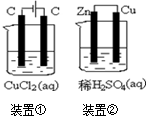
| A.两个装置中都发生了化学变化,都由化学能转变为电能 |
| B.装置②中电流方向是从Zn经导线流入Cu |
| C.反应开始阶段,两个装置中均有氢气产生 |
| D.电极反应式:阳极 2Cl—-2e-→Cl2↑正极 2H++2e-→H2↑ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.若两电极直接连接,a是食盐水,则发生析氢腐蚀 |
| B.若两电极直接连接,则负极反应一定是:Fe-2e→Fe2+ |
| C.若铁接电源负极,石墨接电源正极,a是食盐水,左侧电极上析出的气泡比右侧电极上的多 |
| D.若铁接电源负极,石墨接电源正极,a是氯化铜,铁上有气泡 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
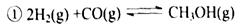


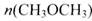 =_________mol。
=_________mol。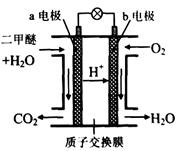
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com