
| 选项 | 条 件 | 离子组 | 离子共存判断及反应的离子方程式 |
| A | 滴加氨水 | Na+、Al3+、Cl-、NO3- | 不能共存, Al3++3OH-═Al(OH)3↓ |
| B | pH=1的溶液 | Fe2+、Al3+、SO42-、MnO4- | 不能共存,5Fe2++MnO4-+8H+ ═Mn2++5Fe3++4H2O |
| C | 由水电离出的H+浓度为1×10-12 mol?L-1 | NH4+、Na+、NO3-、Cl- | 一定能共存, NH4++H2O═NH3?H2O+H+ |
| D | 通入少量SO2气体 | K+、Na+、ClO-、SO42- | 不能共存,2ClO-+SO2+H2O═ 2HClO+SO32- |
| A、A | B、B | C、C | D、C |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯水通过SO2后溶液的酸性增强 |
| B、向明矾溶液中加入过量NaOH溶液会产生大量白色沉淀 |
| C、Na、Fe等金属在一定条件下与水反应都生成H2和对应的碱 |
| D、浓硫酸、浓硝酸在加热条件下能将木炭氧化为二氧化碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、②④⑤ |
| C、①③⑥ | D、①②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
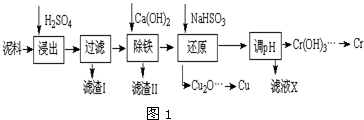
| Fe3+ | Cu2+ | Cr3+ | |
| 开始沉淀pH | 2.1 | 4.7 | 4.3 |
| 完全沉淀pH | 3.2 | 6.7 | a |
查看答案和解析>>
科目:高中化学 来源: 题型:
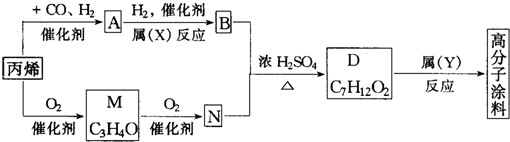
查看答案和解析>>
科目:高中化学 来源: 题型:
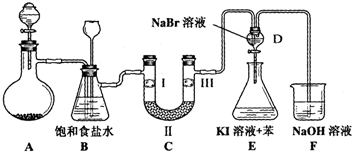
| A | B | C | D | |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com