
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:解答题
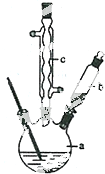 苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要前驱体之一.下面是它的一种实验室合成路线:
苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要前驱体之一.下面是它的一种实验室合成路线: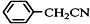 +H2O+H2SO4$\stackrel{100-130℃}{→}$
+H2O+H2SO4$\stackrel{100-130℃}{→}$ +NH4HSO4
+NH4HSO4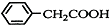 +Cu(OH)2→
+Cu(OH)2→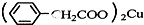 +H2O
+H2O查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16O与18O互为同位素,H218O与D218O互为同素异形体,甲醇、乙二醇与丙三醇互为同系物 | |
| B. | 在SiO2晶体中,一个Si原子和2个O原子形成两个共价键 | |
| C. | 1L0.5mol/L 稀硫酸与1L 1mol/L 氢氧化钠溶液反应放出57.3kJ的热:H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2H2O(1);△H=-114.6 kJ/mol | |
| D. | 碳酸钠水溶液显碱性的原因:CO32-+2H2O?H2CO3+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | pH值减小 | B. | c(H+)和c(OH-)的乘积增大 | ||
| C. | 酸性减弱 | D. | OH-离子浓度减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X2为0.4 mol/L,Y2为1.2 mol/L | B. | Y2为1.6 mol/L | ||
| C. | X2为0.3 mol/L,Z为0.2 mol/L | D. | Z为1.0 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{1}{2{Q}_{2}}$ kJ | B. | Q2kJ | C. | $\frac{1}{3({Q}_{1}+{Q}_{2})}$kJ | D. | $\frac{1}{3{Q}_{1}}$kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | KCl溶液(CaCl2) | 加K2CO3溶液,过滤,再加适量盐酸 |
| B | NaNO3溶液(AgNO3) | 加适量NaCl溶液,过滤 |
| C | NaCl溶液(I2) | 加酒精,分液 |
| D | KBr溶液(Br2) | 加CCl4,分液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除③外 | B. | ④⑤⑥⑦⑧ | C. | ⑤⑦⑧ | D. | ①⑤⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.01mol•L-1HCl | B. | pH=2的H2SO4溶液 | ||
| C. | c(OH)=10-13mol•L-1 | D. | pH=1溶液加水稀释1倍 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com