
| A. | 含有非极性共价键的化合物分子一定是非极性分子 | |
| B. | 原子晶体中只存在非极性共价键 | |
| C. | 冰主要是水分子通过氢键作用而形成的分子晶体 | |
| D. | 若元素R的含氧酸的酸性大于元素Q的含氧酸的酸性,则非金属性R大于Q |
分析 A.如结构不对称,则为极性分子;
B.如为化合物,则含有极性键;
C.通过氢键作用,冰中在四面体中心的每个水分子与在四面体顶角方向的4个相邻的水分子相互吸引,形成有规则排列成的分子晶体;
D.比较非金属性,应用最高价氧化物的水化物.
解答 解:A.含有非极性共价键的化合物分子不一定是非极性分子,如H-O-O-H,O为sp3杂化,结构不对称,为极性分子,故A错误;
B.SiO2为化合物,含有极性键,故B错误;
C.通过氢键作用,冰中在四面体中心的每个水分子与在四面体顶角方向的4个相邻的水分子相互吸引,形成有规则排列成的分子晶体,故C正确;
D.比较非金属性,应用最高价氧化物的水化物,如不是最高价氧化物对应的水化物,则不能根据酸性强弱比较非金属性强弱,故D错误.
故选C.
点评 本题考查较为综合,涉及共价键、氢键以及元素周期率等知识,为高频考点和常见题型,侧重于基本知识的考查,注意相关知识的积累,难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
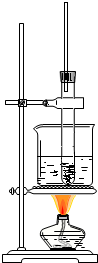 硝基苯是制造染料的重要原料.某同学在实验室里用右图装置制取硝基苯,主要步骤如下:
硝基苯是制造染料的重要原料.某同学在实验室里用右图装置制取硝基苯,主要步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 电负性 离子半径 键的极性 | 熔点 |
| N<O O2->Al3+ C-H<H-O | Al<Al2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
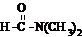 溶于水
溶于水 查看答案和解析>>
科目:高中化学 来源: 题型:解答题
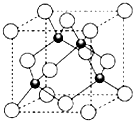 X、Y、Z三元素的原子序数依次增大,三原子的核外最外层电子排布均为4s1.
X、Y、Z三元素的原子序数依次增大,三原子的核外最外层电子排布均为4s1.| r(Zn2+) | r(Z+) | r(S2-) | r(Cl-) | 熔点 | |
| ZnS | ZCl | ||||
| 74pm | 77pm | 184pm | 181pm | 1700℃ | 430℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化钠与浓硫酸混合加热后,撒入二氧化锰即放出氯气 | |
| B. | 过氧化氢中加入几滴氯化铁溶液,可较快放出气体 | |
| C. | 在木炭粉中加入微量氯酸钾,燃烧时极为剧烈 | |
| D. | 用锌与稀硫酸反应制备氢气时,加入少量硫酸铜加快反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇和苯酚均无毒,但都能用于消毒、杀菌 | |
| B. | 乙醇和苯酚均能和金属Na反应置换出氢气 | |
| C. | 苯酚能与甲醛反应制造酚醛树脂 | |
| D. | 乙醇的沸点比乙烷高是因为乙醇分子间可以形成氢键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
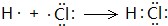 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com