
п���仯������;�㷺������п����п����Ҫ�ɷ���ZnS��Ϊ��Ҫԭ�ϣ��漰����Ҫ��Ӧ�У�
2ZnS(s) + 3O2(g) = 2ZnO(s) + 2SO2(g) 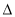 H1=��930 kJ��mol��1
H1=��930 kJ��mol��1
2C(s) + O2(g) = 2CO(g) 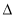 H2=��221 kJ��mol��1
H2=��221 kJ��mol��1
ZnO(s) + CO(g) = Zn(g) + CO2(g) 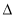 H3=198 kJ��mol��1
H3=198 kJ��mol��1
��ӦZnS(s) + C(s) + 2O2(g)��Zn(g) + CO2(g) + SO2(g) ��
��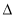 H4= kJ��mol��1��
H4= kJ��mol��1��
��2����Ӧ�����ɵ�CO2��NH3��ϣ���һ�������·�Ӧ�ϳ����أ�
2NH3��g��+CO2��g��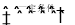 CO��NH2��2��s��+H2O��g����H��0
CO��NH2��2��s��+H2O��g����H��0
���÷�Ӧ��һ���¡������ܱ������ڽ��У��жϷ�Ӧ�ﵽƽ��״̬�ı�־�� ��
a��CO2��H2O(g)Ũ����� b�������������ѹǿ���ٸı�
c��2v(NH3)�� = v(H2O)�� d�������л��������ܶȲ��ٸı�
������߰�����ת���ʣ����Բ�ȡ�Ĵ�ʩ�� ��д��������
��3������п�ɹ㷺����ӡȾýȾ����ľ�ķ�������ZnSO4���ȷֽ�����и��������ʵ������¶ȱ仯��ϵ��ͼ��ʾ��
��700�桫980��ʱ������Ӧ���������ʶ�������ZnO����������÷�Ӧ��2L�ܱ������ڽ��У�10minʱ��������ɵ����������ʵ���Ϊ0.3mol�������ʱ������������������Ϊ ��
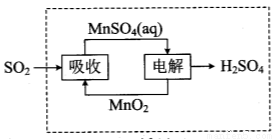
�� ����п�ֽ����ɵ�SO2����ͼ�е�ѭ���ɵõ�H2SO4��ѭ���е�����������Ӧʽ�� ��

 ��˼ά������ҵ��ټ��ִ�ѧ������ϵ�д�
��˼ά������ҵ��ټ��ִ�ѧ������ϵ�д� �����������Ż�ѧϰϵ�д�
�����������Ż�ѧϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ�ʡ��һƽ�а������л�ѧ�Ծ��������棩 ���ͣ�ѡ����
���������м������Ӽ����й��ۼ����ǣ� ��
A��CaCl2 B��H2O C��K2O D��NaOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��������庽����и�һ���������ۻ�ѧ�Ծ��������棩 ���ͣ������
ԭ����ǻ�ѧ�������һ���ش��ס�ij��ȤС��Ϊ�о�ԭ���ԭ���������ͼװ�ã�
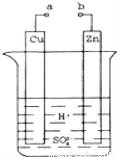
��1��a��b������ʱ���ձ��������� ��
��2��a��b�õ������ӣ�Cu��Ϊԭ���_________�����������������
�缫��ӦʽΪ�� ����Һ��H+����____________
���Cu����Zn������������ܷ�ӦʽΪ�� ��
���������Һ��ΪAgNO3��Һ����ת��0.2mol����ʱ����������CuƬ�����仯Ϊ___ ___g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��������庽����и߶����������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
ijϩ����H2�ӳɺ�IJ����� , ���ϩ���Ľṹʽ������ �� ��
, ���ϩ���Ľṹʽ������ �� ��
A��1�� B��2�� C��3�� D��4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��㶫ʡ�߶������л�ѧ�Ծ��������棩 ���ͣ�ѡ����
���������һ���������Ƹ�Ѫѹ��ҩ�����һ�ֺϳ�·�����£�
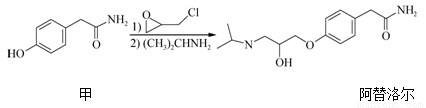
����˵����ȷ����( )
A��������ķ���ʽΪC8H8O2N
B��������������к���2������̼ԭ��
C��һ�������£����������NaOH��Һ��Ũ��ˮ��H2�����Է�����Ӧ
D�����������NaOH�Ҵ���Һ�м��ȿɷ�����ȥ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��㶫ʡ�߶������л�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A�������£���pH��3�Ĵ�����Һϡ�͵�ԭ�����10������Һ��pH��4
B��Ϊȷ��ij��H2A��ǿ�ỹ�����ᣬ�ɲ�NaHA��Һ��pH����pH��7����H2A�������pH��7����H2A��ǿ��
C����0.2000 mol/L NaOH����Һ�ζ�HCl��CH3COOH�Ļ����Һ�����Һ���������Ũ�Ⱦ�ԼΪ0.1 mol/L��,������ʱ����Һ�е���δ����ȫ�к�
D���ں���BaSO4��������Һ�м���Na2SO4���壬c(Ba2+)����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��㶫ʡ�߶������л�ѧ�Ծ��������棩 ���ͣ�ѡ����
NAΪ����٤��������ֵ.����������ȷ����( )
A��1.0L1.0mo1��L��1��NaClOˮ��Һ�к��е�ClO-��ΪNA
B��14g��ϩ�к���������Ϊ2NA
C��22.4LNO2�к�������ΪNA��
D��1mol�������ܽ��ڹ������Ȼ�����Һ�У�����ת����Ϊ3NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��㶫ʡ��һ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��пƬ��ͭƬΪ�缫����ϡ����Ϊ�������Һ��ԭ����У���������ͨ��2mol����ʱ������˵����ȷ����
A��пƬ�ܽ���1mol��ͭƬ������1mol���� B��пƬ������ԭ��Ӧ
C������������SO42-����Ũ�������� D����ع���ʱ������������ͨ�����·����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������ӳظ��и�һ�µڶ����¿���ѧ�Ծ��������棩 ���ͣ�ʵ����
ijͬѧ����ϡ������п��ȡ������ʵ���У����ּ�����������ͭ��Һ�ɼӿ��������������ʡ���ش��������⣺
��1������ͭ��Һ���Լӿ������������ʵ�ԭ����_________��
��2��ʵ����������Na2SO4��MgSO4��HgSO4��K2SO4��4����Һ������ʵ����CuSO4��Һ���������õ���__________��
��3��Ϊ�˽�һ���о�����ͭ�����������������ʵ�Ӱ�죬��ͬѧ���������һϵ��ʵ�顣�����������Ļ����Һ�ֱ���뵽6��ʢ�й���Zn���ķ�Ӧƿ�У��ռ����������壬��¼�����ͬ�������������ʱ�䡣
ʵ�� �����Һ | A | B | C | D | E | F |
4mol��L-1H2SO4��Һ/mL | 30 | V1 | V2 | V3 | V4 | V5 |
����CuSO4��Һ/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
������ɴ�ʵ����ƣ����У�V1=______mL��V9=_____mL��
�ڸ�ͬѧ���ó��Ľ���Ϊ������������CuSO4��Һʱ���������������ʻ�����ߣ����������CuSO4��Һ����һ����ʱ���������������ʷ������½���������������������½�����Ҫԭ��_____________________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com