
| A. | NaCl的电子式: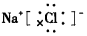 | B. | 硫离子的结构示意图: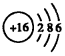 | ||
| C. | 氮气的结构式::N≡N: | D. | 次氯酸的电子式:H:Cl:O: |
分析 A、氯化钠是由钠离子和氯离子构成;
B、硫离子是由硫原子得到两个电子形成的;
C、将电子式中的一对共用电子对用一条短线来代替所得到的式子为结构式;
D、次氯酸中O原子分别与H原子和Cl原子形成共价键.
解答 解:A、氯化钠是由钠离子和氯离子构成,是离子化合物,故电子式为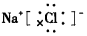 ,故A正确;
,故A正确;
B、硫离子是由硫原子得到两个电子形成的,故核内有16个质子,而核外有18个电子,故结构示意图为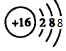 ,故B错误;
,故B错误;
C、将电子式中的一对共用电子对用一条短线来代替所得到的式子为结构式,故氮气的结构式为N≡N,故C错误;
D、HClO为共价化合物,分子中存在1个氧氢键和1个Cl-O键,次氯酸的电子式为 ,故D错误.
,故D错误.
故选A.
点评 本题考查了常见的化学用语,难度不大,应注意电子式的书写规则以及结构式和结构示意图的书写方法,是常考点.


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:选择题
| A. | 简单离子半径大小顺序为:W>Z>R | |
| B. | X2Z2的电子式为: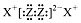 | |
| C. | X2Z的沸点比X2W的沸点高 | |
| D. | Y元素最高价氧化物的水化物浓溶液可以用铝制容器盛装 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
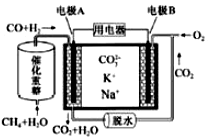
| A. | 电极B上发生的电极反应为:O2+2CO2+4e-=2CO32- | |
| B. | 反应CH4+H2O$\frac{\underline{\;催化剂\;}}{△}$3H2+CO,每消耗1molCH4转移12mol 电子 | |
| C. | 电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O | |
| D. | 电池工作时,CO32-向电极B移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO3与SO2分子空间结构不同,分子中S原子杂化方式也不同 | |
| B. | 乙烯分子中的碳氢键是氢原子的1s轨道和碳原子的一个sp3杂化轨道形成的 | |
| C. | 中心原子采取sp3杂化的分子,其几何构型可能是四面体形或三角锥形或V形 | |
| D. | AB2型的分子空间构型必为直线形 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素 | 元素性质或原子结构的部分信息 |
| W | 元素的离子核外无电子 |
| X | 地壳中含量最多的元素 |
| Y | 元素的离子半径在该周期中最小 |
| Z | Z的单质是淡黄色固体 |
| A. | W与Z形成的化合物在常温下为气体 | |
| B. | Y的最高价氧化物对应的水化物显强碱性 | |
| C. | X和Z形成的常见化合物能形成酸 | |
| D. | 简单氢化物的稳定性:X>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
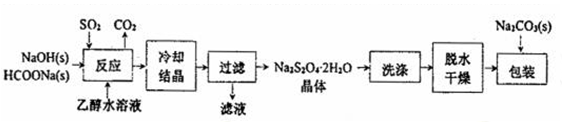
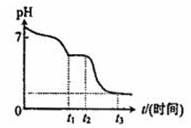

| 绝热恒容(2L ) 密闭容器A | 恒温(T℃)恒容(2L) 密闭容器B | 恒温(T℃)恒压 密闭容器C | |
| 平衡常数K | KA | KB | KC |
| SO2的平衡转化率 | αA | αB | αC |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na$→_{点燃}^{O_{2}}$Na2O2$\stackrel{CO_{2}}{→}$Na2CO3 | B. | FeS2$→_{煅烧}^{O_{2}}$SO3$\stackrel{H_{2}O}{→}$H2SO4 | ||
| C. | NaCl(aq)$\stackrel{电解}{→}$Cl2$→_{△}^{过量Fe}$FeCl2(s) | D. | SiO2$\stackrel{H_{2}O}{→}$H2SiO3$\stackrel{NaOH(aq)}{→}$Na2SiO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com