

���� ���������Ҫ�ɷ���Al2O3��SiO2�ȣ���NaOH��Ӧ�ֱ�Ϊ��Al2O3+2NaOH=2NaAlO2+H2O��SiO2+2NaOH=Na2SiO3+H2O����Ӧ1����Һ�к���NaAlO2��Na2SiO3����CaO��Na2SiO3��ΪCaSiO3����������Һ���е�����ΪNaAlO2��ͨ��A����B��B��������Al2O3����BΪAl��OH��3������AӦ��ΪCO2��������ӦΪ��2AlO2-+CO2+3H2O=2Al��OH��3��+CO32-���Դ˽����⣮
��� �⣺���������Ҫ�ɷ���Al2O3��SiO2�ȣ���NaOH��Ӧ�ֱ�Ϊ��Al2O3+2NaOH=2NaAlO2+H2O��SiO2+2NaOH=Na2SiO3+H2O����Ӧ1����Һ�к���NaAlO2��Na2SiO3����CaO��Na2SiO3��ΪCaSiO3����������Һ���е�����ΪNaAlO2��ͨ��A����B��B��������Al2O3����BΪAl��OH��3������AӦ��ΪCO2��������ӦΪ��2AlO2-+CO2+3H2O=2Al��OH��3��+CO32-��
��1�����������Ҫ�ɷ���Al2O3��SiO2�ȣ���NaOH��Ӧ��Al2O3+2NaOH=2NaAlO2+H2O��SiO2+2NaOH=Na2SiO3+H2O����Һ���к��й����ơ�ƫ�����ƣ�����CaO�������������ƣ���������������Ʒ�Ӧ���ɹ���Ƴ�����
�ʴ�Ϊ��Al2O3+2NaOH=2NaAlO2+H2O��SiO2+2NaOH=Na2SiO3+H2O��CaSiO3��
��2����Ӧ2��Ӧ���еIJ�������������Һ��ӦΪ���˲������ʴ�Ϊ�����ˣ�
��3���ɹ������̿�֪��BΪ����������������AΪ������̼����Һ����Ҫ��ƫ�����ƣ�ƫ��������Һͨ�������̼����������������̼���ƣ���Ӧ����ʽΪ��2AlO2-+CO2+3H2O=2Al��OH��3��+CO32-��
�ʴ�Ϊ��CO2��2AlO2-+CO2+3H2O=2Al��OH��3��+CO32-��
��4������������Ļ�ѧ����ʽΪ2Al2O3$\frac{\underline{\;���\;}}{\;}$4Al+3O2�����ʴ�Ϊ��2Al2O3$\frac{\underline{\;���\;}}{\;}$4Al+3O2����
���� ���⿼����������ᴿ��Ϊ��Ƶ���㣬���շ��������з����ķ�Ӧ���������뷽��Ϊ���Ĺؼ������ط�����ʵ�������Ŀ��飬ע��Ԫ�ػ�����֪ʶ��ʵ�鼼�ܵ��ۺ�Ӧ�ã���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ij���ʵ���ҺpH��7���������һ�������ǿ�������� | |
| B�� | pH=4.5�ķ���֭��c��H+����pH=6.5��ţ����c��H+����100�� | |
| C�� | ��1L0.1mol•L-1��Ba��OH��2��Һϡ��Ϊ2L��pH=12 | |
| D�� | pH=8��NaOH��Һϡ��100������pH=6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
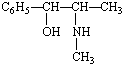 ��������������ӡ���
��������������ӡ���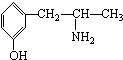 B��
B��
 D��
D��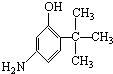 E��
E��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | pH��7�Ľ�ˮ��Ϊ���� | |
| B�� | �����ƿ������Ʊ�ľ�ķ���� | |
| C�� | ˮ�ࡢ�մɡ����������ڹ����β�Ʒ | |
| D�� | ��������ʹ��ȼúȡů�ᵼ���������γ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
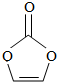
| A�� | ����ʽΪC3H2O3 | B�� | ������ֻ���м��Լ� | ||
| C�� | �����к�6���Ҽ� | D�� | ��̼ԭ���ӻ��ķ�ʽ��ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ƽ��������Ӧ�����ƶ� | B�� | A��ת�������� | ||
| C�� | D������������� | D�� | a+b��c+d |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
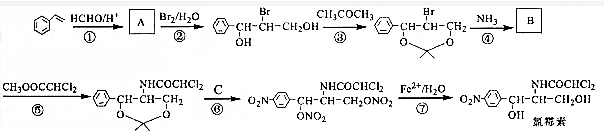
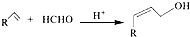
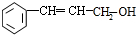 ��C���������ᣮ
��C���������ᣮ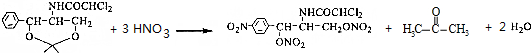 ��
��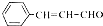 �ĺϳ�·�ߣ�
�ĺϳ�·�ߣ��鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com