
| 选项 | 实验操作 | 现象 | 结论 |
| A | 用湿润的蓝色石蕊试纸检验某气体 | 试纸变红 | 气体呈碱性 |
| B | 铁粉中加入新制氯水,充分反应后,滴入KSCN溶液 | 溶液呈红色 | 铁粉被氧化成Fe3+ |
| C | 向Mg(OH)2的上层清液中滴加MgCl2溶液 | 沉淀变成白色 | Qc[Mg(OH)2]<Ksp[Mg(OH)2] |
| D | 将少量溴水分别滴入FeCl2溶液、NaI溶液中,再分别滴加CC14,振荡静置 | 下层分别为无色和紫红色 | 氧化性:Br2>Fe3+>I2 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.用湿润的蓝色石蕊试纸变红,不能检验碱性气体;
B.滴入KSCN溶液变红,说明生成三价铁;
C.上层清液中滴加MgCl2溶液,发生沉淀生成;
D.溴水分别滴入FeCl2溶液、NaI溶液,均发生氧化还原反应,分别生成铁离子、碘.
解答 解:A.由检验氨气利用红色的石蕊试纸,试纸变蓝为氨气可知,则不能用湿润的蓝色石蕊试纸检验碱性气体,故A错误;
B.滴入KSCN溶液变红,说明生成三价铁,则Fe与氯气反应生成氯化铁,铁粉被氧化成Fe3+,故B正确;
C.上层清液中滴加MgCl2溶液,发生沉淀生成,则Qc[Mg(OH)2]>Ksp[Mg(OH)2],故C错误;
D.溴水分别滴入FeCl2溶液、NaI溶液,均发生氧化还原反应,分别生成铁离子、碘,分别滴加CC14,振荡静置,下层分别为无色和紫红色,但氧化性Br2>Fe3+、Br2>I2,不能说明Fe3+、I2的氧化性,故D错误;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、氧化还原反应、沉淀生成、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验评价性分析,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
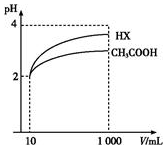 25℃时,三种酸的电离平衡常数如表所示.
25℃时,三种酸的电离平衡常数如表所示.| 化学式 | CH3COOH | HClO | H3PO3 |
| 名称 | 醋酸 | 次氯酸 | 亚磷酸 |
| 电离平衡常数(25℃) | 1.8×10-5 | 3.0×10-8 | K1=8.3×10-3 K2=5.6×10-6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2:1:2 | B. | 1:1:1 | C. | 5:5:4 | D. | 7:7:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液溴需用少量水液封 | |
| B. | NaOH固体最好盛放在塑料瓶中 | |
| C. | FeSO4溶液需加入少量硫酸和铁粉 | |
| D. | 浓硝酸用带橡胶塞的棕色细口瓶盛放 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 日光灯管破碎,只需收集散落的汞即可 | |
| B. | 金属镁失火,应采用泡沫灭火器灭火 | |
| C. | 钡离子中毒,可以通过服用碳酸钠溶液解毒 | |
| D. | 烧碱溶液溅到皮肤上,应立即用大量的水冲洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | |
| Z | W | Q |
| A. | X、W能分别与钠形成摩尔质量相同且阴、阳离子个数比为1:2的化合物 | |
| B. | X和Z只能形成一种化合物 | |
| C. | 氧化物对应的水化物酸性:W<Q | |
| D. | 原子半径大小关系:Q>W>Z>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 异丁烷的二氯代物 | |
| B. | 分子式为C6 H14的有机物 | |
| C. | 甲酸正丙酯属于酯的同分异构体 | |
| D. | 分子式为C5H10O2并能与饱和NaHCO3溶液反应放出气体的有机物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com