
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |


科目:高中化学 来源: 题型:
| A、σ键能单独形成,而π键一定不能单独形成 |
| B、σ键可以绕键轴旋转,π键一定不能绕键轴旋转 |
| C、HCl 分子中的σ键是由一个原子的s轨道和另一个原子的p轨道以“头碰头”方式重叠构建而成的 |
| D、气体单质中一定存在σ键,可能存在π键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 450 | 750 | 800 | 900 |
| 平衡常数 | 3.5 | 1.8 | 1.0 | 0.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 结构或性质信息 |
| A | 原子核外有一个未成对电子,其氢化物与水分子间能形成氢键 |
| B | 原子核外M层电子数是N层电子数的4倍 |
| C | 是使用最为广泛的合金的主要成分 |
| D | 原子各内层电子均已饱和,最外层电子数为1 |
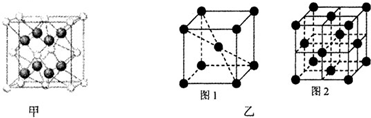
查看答案和解析>>
科目:高中化学 来源: 题型:
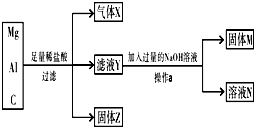 用镁粉、铝粉和炭粉组成的混合物进行如图所示实验,回答下列问题.
用镁粉、铝粉和炭粉组成的混合物进行如图所示实验,回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、不可将温度计当搅拌棒使用,也不可靠在容器内壁上 |
| B、搅拌时,环形玻璃搅拌棒应上下移动 |
| C、测量反应混合液的温度时要随时读取温度,记录下最高温度 |
| D、为了使反应完全,必须保证酸和碱恰好完全反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
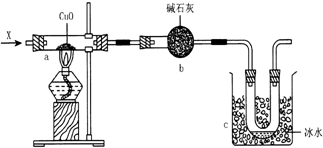
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.6a g |
| B、(a-1.6)g |
| C、(a-3.2)g |
| D、1.6 g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③ | B、①② | C、①②④ | D、②④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com