
 某同学用铁、铜作为电极,稀硫酸作为电解液组成原电池,如图所示,完成下列空格.(涉及到电极填写具体物质的元素符号)
某同学用铁、铜作为电极,稀硫酸作为电解液组成原电池,如图所示,完成下列空格.(涉及到电极填写具体物质的元素符号)分析 (1)根据电极材料的活泼性判断正负极;根据生成物判断;根据现象写电极反应式;
(2)根据电子的流向判断电流的流向;
(3)根据氢气与电子转移的关系式计算;根据氢气与铁的关系式计算.
解答 解:(1)铁的活泼性大于铜,所以铜是正极;正极上氢离子得电子生成氢气,所以看到的现象是有气泡生成,发生还原反应.
故答案为:铜极;有气泡产生;2H++2e-=H2↑;
(2)电子的流向是从负极沿导线到正极,电流的方向与电子的流向相反,
故答案为:铜极;铁极;
(3)Fe+H2SO4 =FeSO4 +H2↑ 转移电子
56g 22.4L 2mol
11.2g 4.48L 0.4mol
故答案为:0.4;11.2.
点评 本题考查原电池原理,侧重考查电极反应式书写、电子流向及阴阳离子移动方向等知识点,电解质溶液中阴阳离子移动方向是学习难点,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
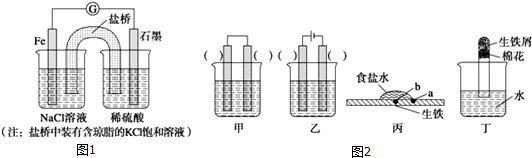
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
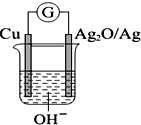 普通水泥在固化过程中自由水分子减少,并且溶液呈碱性.根据这一物理化学特点,科学家发明了利用原电池原理测定水泥初凝时间.此法的原理如图所示,反应的总方程式为2Cu+Ag2O═Cu2O+2Ag.下列有关说法错误的是( )
普通水泥在固化过程中自由水分子减少,并且溶液呈碱性.根据这一物理化学特点,科学家发明了利用原电池原理测定水泥初凝时间.此法的原理如图所示,反应的总方程式为2Cu+Ag2O═Cu2O+2Ag.下列有关说法错误的是( )| A. | Ag2O/Ag电极为正极 | |
| B. | Cu电极为负极 | |
| C. | 电池工作时,OH-向Ag2O/Ag电极移动 | |
| D. | 电池工作时,有1 mol Cu2O生成时,电路中有2 mol电子通过 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 某校研究性学习小组用相同大小的铜片和锌片为电极研究水果电池(如图所示),得到的实验数据如表所示:
某校研究性学习小组用相同大小的铜片和锌片为电极研究水果电池(如图所示),得到的实验数据如表所示:| 实验编号 | 水果种类 | 电极间距离/cm | 电流大小/?A |
| ① | 西红柿 | 1 | 98.7 |
| ② | 西红柿 | 2 | 72.5 |
| ③ | 苹果 | 2 | 27.2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com