
分析 (1)发生反应为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,利用差量法计算出分解的碳酸氢钠的质量;
(2)最终得到的固体为碳酸钠,根据Na元素守恒计算出所得溶液的浓度.
解答 解:(1)2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O△m
168 62
xg 16.8g-13.7g=3.1g
则:x=$\frac{168×3.1g}{62}$=8.4g,
答:NaHCO3发生分解反应的质量为8.4g;
(2)根据2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O可知,最终得到的固体为碳酸钠,则所得溶液中碳酸钠的物质的量为:n(Na2CO3)=$\frac{1}{2}$n(NaHCO3)=$\frac{16.8g}{84g/mol}$×$\frac{1}{2}$=0.1mol,所得溶液的浓度为:c(NaHCO3)=$\frac{0.1mol}{1L}$=0.1mol/L,
答:该溶液溶质的物质的量浓度是0.1 mol/L.
点评 本题考查化学方程式的计算,题目难度不大,明确发生反应的实质为解答关键,注意掌握差量法在化学计算中的应用,试题培养了学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | 乙炔 | B. | 乙烯 | C. | 丁二烯 | D. | 丙炔 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
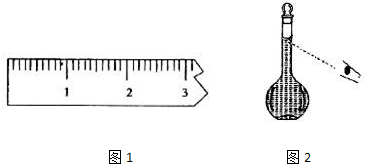
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2固体中阳离子与阴离子的个数比为1:1 | |
| B. | 从试剂瓶中取出并切下的未使用的钠可放回原试剂瓶中 | |
| C. | 将Na投入饱和Na2CO3溶液中,会导致溶液质量增加 | |
| D. | 金属Na失火,可用CO2灭火 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 静电除尘器除去空气中的飘尘是利用胶体粒子的带电性而加以除去 | |
| B. | 溶液和胶体均为呈电中性的分散系 | |
| C. | FeCl3溶液和Fe(OH)3胶体的本质区别是后者可以产生丁达尔现象 | |
| D. | 由于胶粒之间的排斥作用,胶粒不易聚集成大的颗粒,所以胶体比较稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2CH4(g)+4O2(g)→2CO2(g)+4H2O(1);△H=+890kJ•mol-1 | |
| B. | CH4(g)+2O2(g)→CO2(g)+2H2O(1);△H=+445kJ•mol-1 | |
| C. | CH4(g)+2O2(g)→CO2(g)+2H2O(1);△H=+890kJ•mol-1 | |
| D. | $\frac{1}{2}$CH4(g)+O2(g)=$\frac{1}{2}$CO2(g)+H2O(1);△H=-445kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  | B. |  | ||
| C. |  | D. | 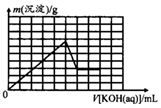 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
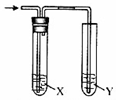 用图所示装置进行相关实验,能达到实验目的是( )
用图所示装置进行相关实验,能达到实验目的是( )| 实验 | 试剂X | 试剂Y | |
| A | 检验乙醇与浓硫酸共热产生的乙烯 | NaHSO3溶液 | KMnO4酸性溶液 |
| B | 检验CO2和SO2混合气体中的CO2 | 品红溶液 | 澄清的石灰水 |
| C | 除去Cl2中混有的HCl,并验证Cl2的漂白性 | 饱和NaCl溶液 | 品红溶液 |
| D | 通入 HCl,验证非金属性Cl>C>Si | NaHCO3溶液 | Na2 SiO3溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com