
| A、三聚氰胺是劣质蛋白质 |
| B、在检测条件下三聚氰胺可以转化为蛋白质 |
| C、三聚氰胺中氮元素的含量高于蛋白质中氮的含量 |
| D、三聚氰胺及蛋白质中的氮元素在检测条件下可以转化生成相同的物质 |
| 该元素的相对原子质量×原子个数 |
| 化合物的相对分子质量 |
| 14×6 |
| 126 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
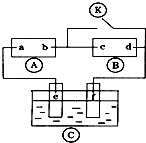 如图
如图 为直流电源,
为直流电源, 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸, 为电镀槽.接通电路后发现
为电镀槽.接通电路后发现 上的c点显红色.为实现铁上镀锌,接通
上的c点显红色.为实现铁上镀锌,接通 后,使c、d两点短路.下列叙述不正确的是( )
后,使c、d两点短路.下列叙述不正确的是( )| A、a为直流电源的正极 |
| B、c极发生的反应为2H++2e-=H2↑ |
| C、f电极为锌板 |
| D、e极发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Z>X>W>Y |
| B、Z>W>Y>X |
| C、X>Y>W>Z |
| D、X>Y>Z>W |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 实验室制取并收集氨气 |
B、 制取SO2并检验SO2的漂白性 |
C、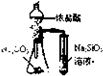 比较氯碳硅三种元素的非金属性强弱 |
D、 除去CO2中的HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CaC2能水解:CaC2+2H2O═Ca(OH)2+C2H2↑,则Al4C3也能水解:Al4C3+12H2O═4Al(OH)3↓+3CH4↑ |
| B、O2与Cu加热反应生成CuO,则S与Cu加热反应生成CuS |
| C、根据化合价Fe3O4可表示为FeO?Fe2O3,则Fe3I8也可表示为FeI2?2FeI3 |
| D、SO2通入BaCl2溶液中不产生沉淀,则SO2通入Ba(NO3)2溶液中也不产生沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 纯铜在工业上主要用来制造导线、电器元件等,铜能形成+1和+2价的化合物.回答下列问题:
纯铜在工业上主要用来制造导线、电器元件等,铜能形成+1和+2价的化合物.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
 已知A、B、C为中学化学中常见的单质.室温下,A为固体,B和C均为气体.在适宜的条件下,它们可以按如图进行反应.回答下列问题:
已知A、B、C为中学化学中常见的单质.室温下,A为固体,B和C均为气体.在适宜的条件下,它们可以按如图进行反应.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢气和氯气反应生成氯化氢气体的热化学方程式是H2(g)+Cl2(g)═2HCl(g) |
| B、氢气与氯气反应生成2mol的氯化氢气体,反应的△H=183 kJ?mol-1 |
| C、氢气与氯气反应生成2mol氯化氢气体,反应的△H=-183 kJ?mol-1 |
| D、氢气与氯气反应生成1mol氯化氢气体,反应的△H=-91.5 kJ?mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com