解:(1)高锰酸钾具有强氧化性,在酸性环境下,能将草酸氧化为二氧化碳,同时自身被还原为锰离子,
根据得失电子数相等配平方程式,即:5C
2O
42-+2MnO
4-+6H
+=10CO
2↑+2Mn
2++8H
2O
,故答案为:5,2,6,10CO
2,2,8;
(2)碱滴定酸时用酚酞试液作指示剂,所以要在滴定液中滴加酚酞试液,故答案为:滴加酚酞试液;
(3)①用于配制溶液的250mL容量瓶、定容使用胶头滴管,故答案为:250mL容量瓶、胶头滴管;
②高锰酸钾本身具有颜色,在滴定草酸的过程中可以担当指示剂的角色,当最后一滴滴入溶液中,溶液恰好变紫红色,且30s内不退色,此时便是滴定终点,
故答案为:KMnO
4最后一滴滴入溶液,溶液恰好变紫红色,且30s内不退色,此时便是滴定终点;
③根据5C
2O
42-+2MnO
4-+6H
+=10CO
2↑+2Mn
2++8H
2O知,草酸根离子的物质的量=
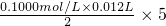
×10=0.3mol,
根据氢氧化钠的物质的量计算草酸的物质的量=
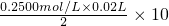
=0.025mol,
根据碳原子守恒得KH
3(C
2O
4)
2?2H
2O的物质的量=
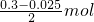
=0.1375mol,
纯度=
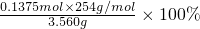
=98.%,
故答案为:0.3mol,98.1%;
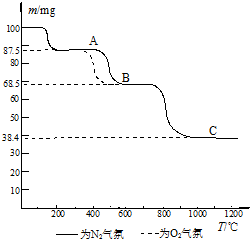
(4)①加热过程中,草酸钙分解分三步,第1步反应为CaC
2O
4?xH
2O失去结晶水生成CaC
2O
4,第2步反应为CaC
2O
4分解生成CaCO
3与碳的氧化物,第3步,继续加热固体,碳酸钙分解生成氧化钙和二氧化碳,
所以C的固体是CaO,故答案为:CaO;
②在氧气氛围内,第2步产生的一氧化碳和氧气反应生成的二氧化碳,第2步产生的二氧化碳抑制碳酸钙分解,所以氧气存在时不利于第3步反应进行,
故答案为:氧气存在时第2步反应产生二氧化碳会抑制碳酸钙分解反应的进行.
分析:(1)酸性条件下,草酸根离子能被高锰酸根离子氧化生成二氧化碳,同时高锰酸根离子被还原生成锰离子;
(2)用酚酞试液检验测定终点;
(3)①根据各仪器的作用选取仪器;
②高锰酸钾本身具有颜色,在滴定过程中可以担当指示剂的角色;
③根据草酸根离子和高锰酸钾之间的关系式计算;
(4)第1步反应为CaC
2O
4?xH
2O失去结晶水生成CaC
2O
4,第2步反应为CaC
2O
4分解生成CaCO
3与碳的氧化物,第3步,继续加热固体,碳酸钙分解生成氧化钙和二氧化碳.
点评:本题考查物质的量的有关计算及物质的确定,明确图象中曲线拐折的含义是解本题的关键,注意(3)中和高锰酸钾反应的草酸根离子包含草酸中的,为易错点,难度较大.


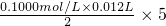 ×10=0.3mol,
×10=0.3mol,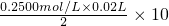 =0.025mol,
=0.025mol,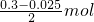 =0.1375mol,
=0.1375mol,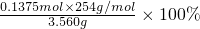 =98.%,
=98.%,