
| A. | 12 | B. | 14 | C. | 16 | D. | 18 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
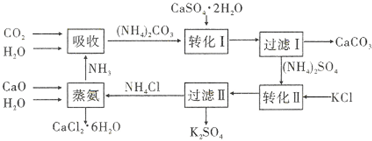
| 温度(℃) | 0 | 20 | 60 |
| K2SO4溶解的量(g) | 7.4 | 11.1 | 18.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
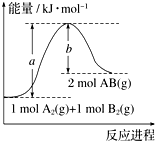 图象法是研究化学反应的焓变的一种常用方法.已知化学反应A2(g)+B2(g)═2AB(g)的能量变化曲线如图所示,则下列叙述中正确的是( )
图象法是研究化学反应的焓变的一种常用方法.已知化学反应A2(g)+B2(g)═2AB(g)的能量变化曲线如图所示,则下列叙述中正确的是( )| A. | 每生成2 mol AB时吸收(a-b) kJ能量 | |
| B. | 该反应热△H=+(a-b) kJ•mol-1 | |
| C. | 该反应中反应物的总能量高于生成物的总能量 | |
| D. | 断裂1 mol A-A和1 mol B-B键时放出a kJ能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
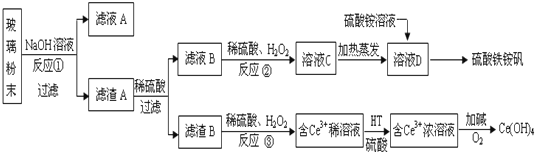
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑥ | B. | ①②③ | C. | ②③⑤ | D. | ①②⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用可见光束可以鉴别红褐色的氢氧化铁胶体和溴水,是因为溶液与胶体的本质区别是能否发生丁达尔效应 | |
| B. | 分散系是一种物质分散到另一种物质中形成的混合体系 | |
| C. | 氢氧化铁胶体具有吸附性,能吸附水中悬浮颗粒并沉降,因而常用于净水 | |
| D. | 淀粉溶液和蛋白质溶液是溶液,不可能是胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
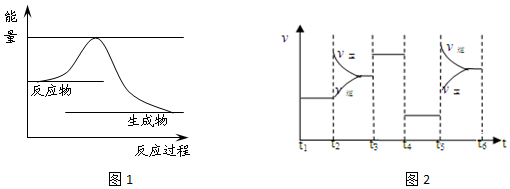
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将铜丝插入稀硝酸中:Cu+4H++2NO3-═Cu2++2NO2↑+H2O | |
| B. | 向Fe2(SO4)3溶液中加入过量铁粉:Fe3++Fe═2Fe2+ | |
| C. | 向NaAlO2溶液中通入过量CO2 制Al(OH)3:CO2+AlO2-+2H2O=Al(OH)3↓+HCO3- | |
| D. | 用氨水吸收足量的SO2气体:2OH-+SO2=SO32-+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com