
| A、1 mol AlCl3在熔融状态时离子总数为0.4NA |
| B、标准状况下,2.24L苯中含有的C-H键的数目为0.6NA |
| C、2.2g分子式为 2H218O的水中含有的中子数为1.2 NA |
| D、电解饱和食盐水时,当阴极产生H2 22.4L时,电路中转移的电子数为2NA |
| 2.2 |
| 22 |


 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案科目:高中化学 来源: 题型:
| A、实验剩余的钠可放入废液缸中 |
| B、用NaOH溶液洗涤并灼烧铂丝后,再进行焰色反应 |
| C、大量氯气泄漏时,迅速离开现场,并逆风前往安全区域疏散 |
| D、不慎洒出的酒精在桌上着火时,立即用大量水扑灭 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用电动汽车代替燃油汽车 |
| B、将聚乙烯等塑料垃圾深埋或倾入海中 |
| C、用沼气、太阳能、风能等能源替代化石燃料 |
| D、大力实施矿物燃料的脱硫脱硝技术以减少SO2、NOx的排放 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X、W、U的最高价氧化物对应的水化物酸性由强到弱的顺序为:U>W>X |
| B、Y、Z元素的单质作电极,在NaOH溶液中构成原电池,Z电极上产生大量气泡 |
| C、室温下,0.05 mol/L U的气态氢化物的水溶液的pH>1 |
| D、Y、Z、U元素的简单离子半径由大到小的顺序:Y>Z>U |
查看答案和解析>>
科目:高中化学 来源: 题型:
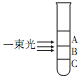 氯化银胶体中的分散质粒子实际上是一个个由很多“AgCl”结合而成的集合体.向盛有NaCl溶液的试管中滴加AgNO3溶液,静置后用一束光照射试管,发现试管的三个不同区域中只有一个区域具有明显的丁达尔效应,则下列分析正确的是( )
氯化银胶体中的分散质粒子实际上是一个个由很多“AgCl”结合而成的集合体.向盛有NaCl溶液的试管中滴加AgNO3溶液,静置后用一束光照射试管,发现试管的三个不同区域中只有一个区域具有明显的丁达尔效应,则下列分析正确的是( )| A、该区域是A,该区域中AgCl的直径最小 |
| B、该区域是B,该区域中AgCl的直径介于A、C区域之间 |
| C、该区域是C,该区域中AgCl的直径最大 |
| D、各区域AgCl的大小都相同,但只有B区域中分散质的大小介于1~100 nm之间 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、32g O3所含有的原子数为2NA |
| B、18g NH4+中所含的离子数为NA |
| C、22.4LCO2所含的原子数为3NA |
| D、1 mol/L碳酸钠溶液中所含钠离子的总数为2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、明矾净水原理:Al3++3H2O=Al(OH)3↓+3H+ |
| B、向偏铝酸钠溶液中通入少量的CO2气体 AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- |
| C、向澄清石灰水中滴加盐酸 Ca(OH)2+2H+=Ca2++2H2O |
| D、向碳酸氢钙溶液中加入过量的氢氧化钠溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
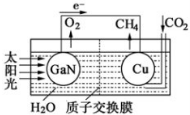
| ||

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、77.6 kJ |
| B、-77.6 kJ?mol-1 |
| C、+77.6kJ?mol-1 |
| D、-886.8kJ?mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com